найдите массу сульфида железа который образуется при взаимодействии 112г железа с серой нужна пропорция
Ответы
Ответ дал:
0
ну вот как-то так...)))))
Приложения:
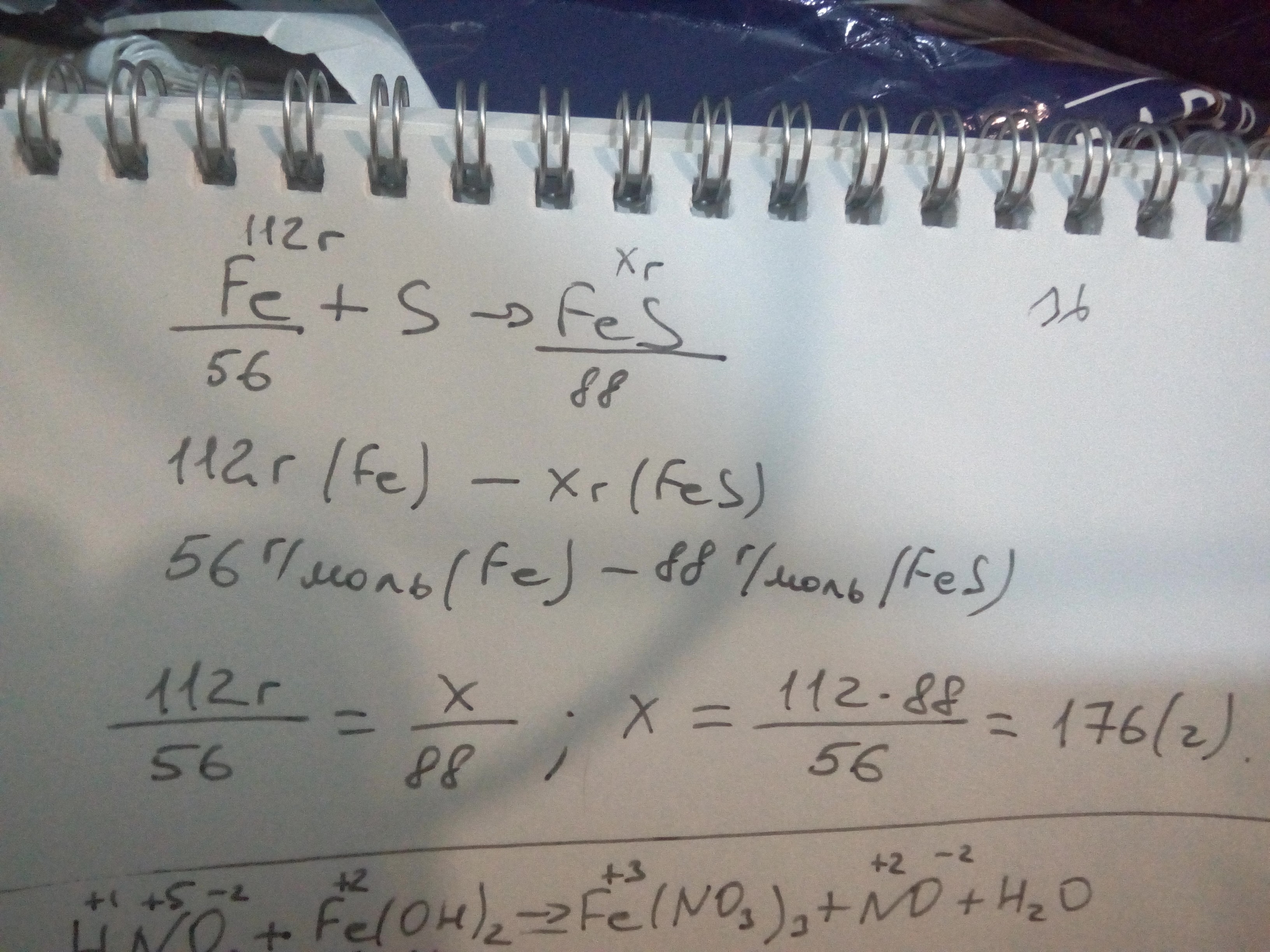
Ответ дал:
0
Дано:
m(Fe) = 112 г
Найти:
m(FeS) -?
М(Fe) = 56 г/моль
M(FeS) = 88 г/моль
Fe+S = FeS
n(Fe) = 112 г/56 г/моль =2 моль
n(FeS)=n(Fe) = 2 моль
m(Fe) = n(Fe)*M(Fe) = 2 моль*88 г/моль = 176 г
Второй способ:
112 г х г
Fe + S = FeS
1 моль 1 моль
56 г 88 г
112:56=х:88
х=176 г
Ответ: 176 г
m(Fe) = 112 г
Найти:
m(FeS) -?
М(Fe) = 56 г/моль
M(FeS) = 88 г/моль
Fe+S = FeS
n(Fe) = 112 г/56 г/моль =2 моль
n(FeS)=n(Fe) = 2 моль
m(Fe) = n(Fe)*M(Fe) = 2 моль*88 г/моль = 176 г
Второй способ:
112 г х г
Fe + S = FeS
1 моль 1 моль
56 г 88 г
112:56=х:88
х=176 г
Ответ: 176 г
Приложения:
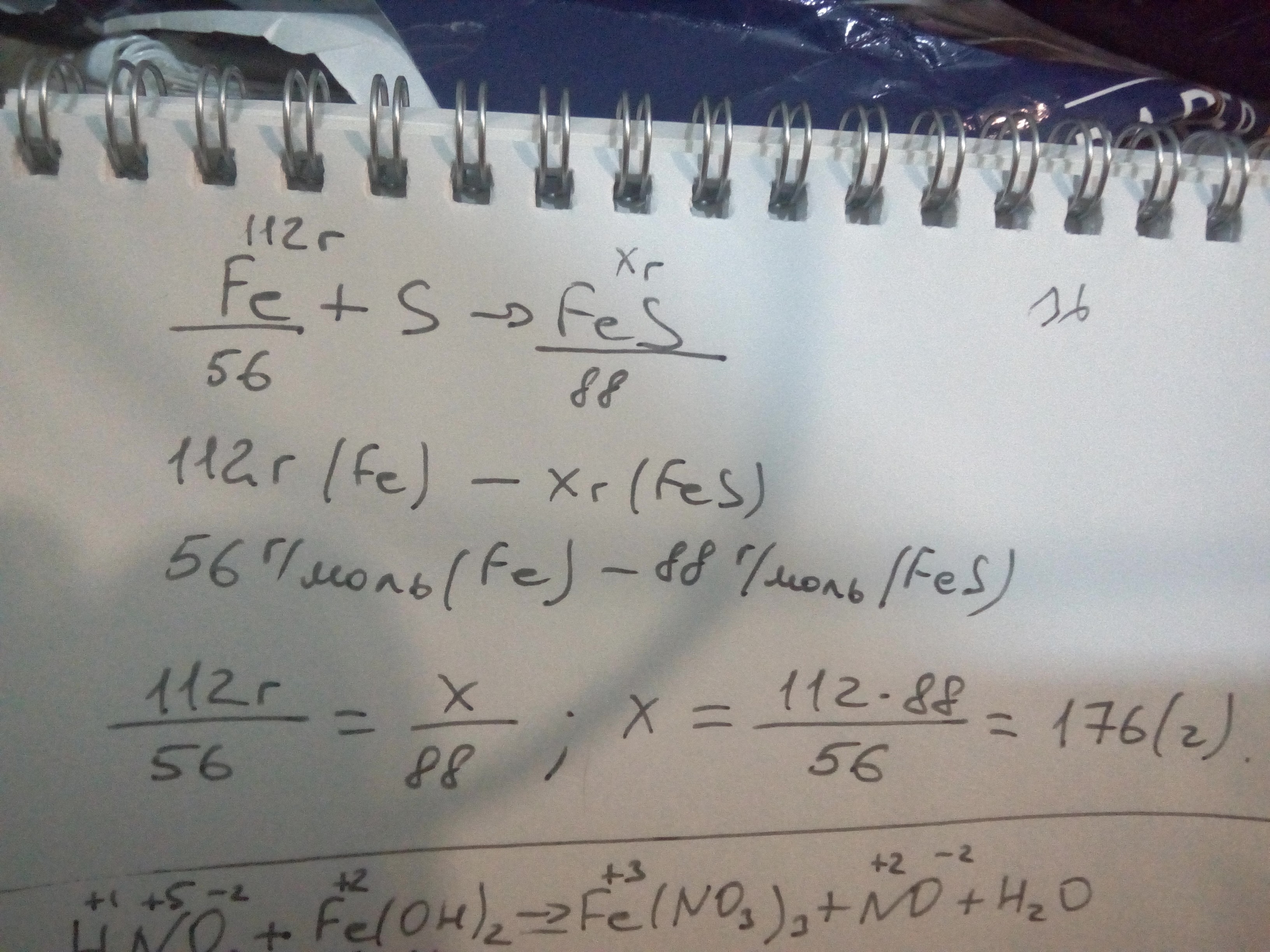
Вас заинтересует
2 года назад
2 года назад
7 лет назад
10 лет назад
10 лет назад
10 лет назад
10 лет назад