в реакции с азотной кислатой прореогировало 0,1 моль оксида меди (2), найти массу и количества вещества нетрота меди(2),получившегося реакцыи
Ответы
Ответ дал:
0
Вот решение! Все очень легко и просто!
Приложения:
Ответ дал:
0
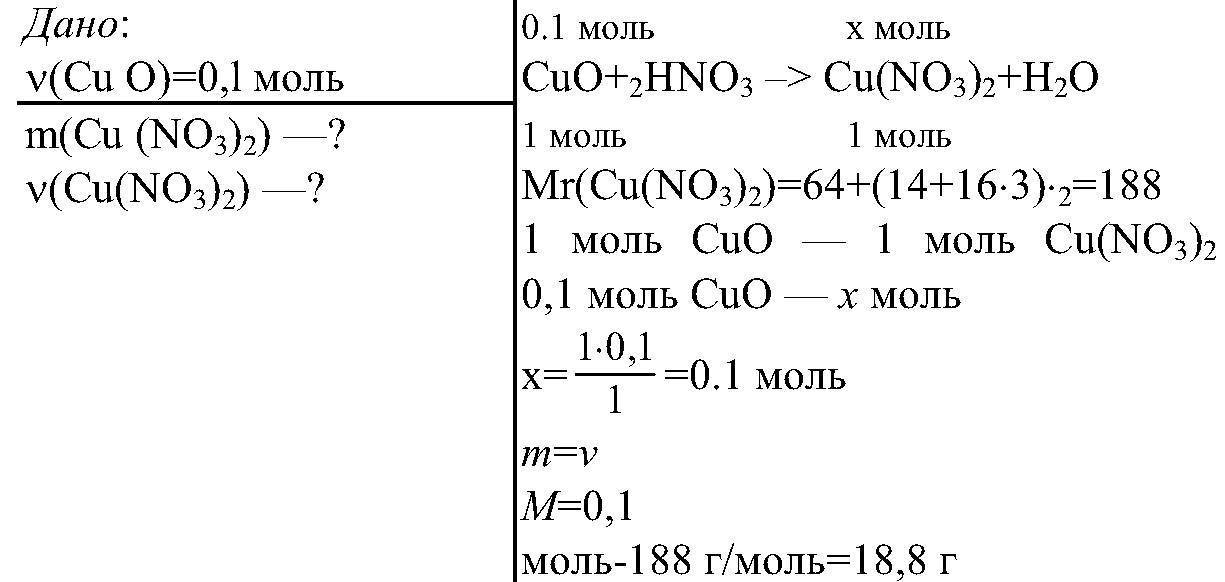
0,1 моль Х г, Х моль
CuO + 2HNO3 -> Cu(NO3)2 + H2O
n=1 моль n=1 моль
М = 188 г/моль
m=188 г
0,1 моль CuO - Х г Cu(NO3)2
1 моль CuO - 188 г Cu(NO3)2
m(Cu(NO3)2) = 0,1 * 188 / 1 = 18,8 г
n(Cu(NO3)2) = m(Cu(NO3)2) / M(Cu(NO3)2) = 18,8 / 188 = 0,1 моль
CuO + 2HNO3 -> Cu(NO3)2 + H2O
n=1 моль n=1 моль
М = 188 г/моль
m=188 г
0,1 моль CuO - Х г Cu(NO3)2
1 моль CuO - 188 г Cu(NO3)2
m(Cu(NO3)2) = 0,1 * 188 / 1 = 18,8 г
n(Cu(NO3)2) = m(Cu(NO3)2) / M(Cu(NO3)2) = 18,8 / 188 = 0,1 моль
Приложения:

Вас заинтересует
2 года назад
2 года назад
10 лет назад
10 лет назад
10 лет назад