Решите задачу по химии 30 баллов.Срочно!!!
Какую массу оксида кальция можно получить при прокалывании 300г. известняка содержащего 5%примеси(решение на фото)
Ответы
Ответ дал:
0
https://pp.userapi.com/c845321/v845321392/542ff/6OvVgHaHHn8.jpg
Приложения:
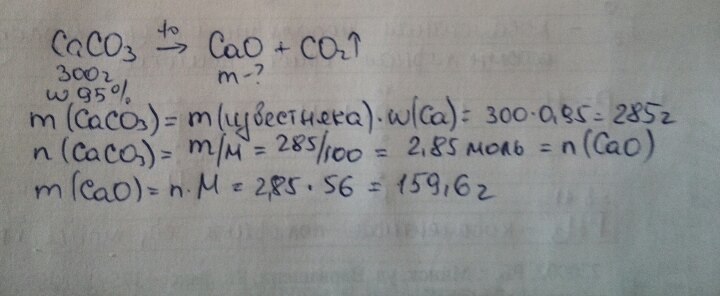
Ответ дал:
0
и что это
Ответ дал:
0
Ваше решение. Не открывается?
Ответ дал:
0
Добавила фото по ссылке
Ответ дал:
0
спасибо
Ответ дал:
0
дано
m извест (CaCO3) = 300 g
W(прим) = 5%
--------------------------
m(CaO)-?
m чист(CaCO3) = 300 - ( 300*5%/100%) = 285 g
CaCO3--t--> CaO+ CO2
M(CaCO3) = 100 g/mol
n(CaCO3) = m/M = 285 / 100 = 2.85 mol
n(CaCO3) = n(CaO) = 2,85 mol
M(CaO) = 56 g/mol
m(CaO) = n*M = 2.85 * 56 = 159.6 g
ответ 159.6 г
m извест (CaCO3) = 300 g
W(прим) = 5%
--------------------------
m(CaO)-?
m чист(CaCO3) = 300 - ( 300*5%/100%) = 285 g
CaCO3--t--> CaO+ CO2
M(CaCO3) = 100 g/mol
n(CaCO3) = m/M = 285 / 100 = 2.85 mol
n(CaCO3) = n(CaO) = 2,85 mol
M(CaO) = 56 g/mol
m(CaO) = n*M = 2.85 * 56 = 159.6 g
ответ 159.6 г
Приложения:
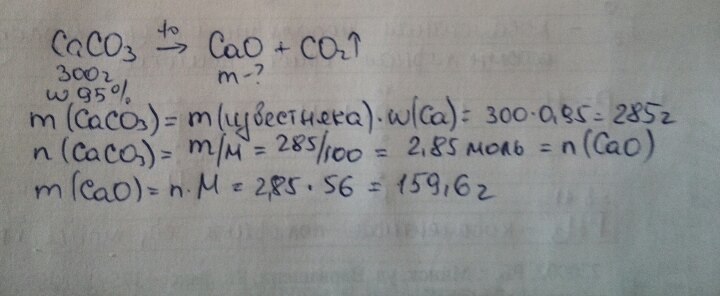
Вас заинтересует
2 года назад
3 года назад
3 года назад
9 лет назад
9 лет назад
10 лет назад