NA2O+2HCL=2NACL+H2O вычислить какая масса соляной кислоты затратится на реакцию с 31 граммами оксида натрия
Ответы
Ответ дал:
0
Дано:
m (Na₂O) = 31 г.
Найти:
m (HCl) — ?
Решение:
↓ [РЕШЕНИЕ И ОТВЕТ ВО ВЛОЖЕНИИ] ↓
Приложения:
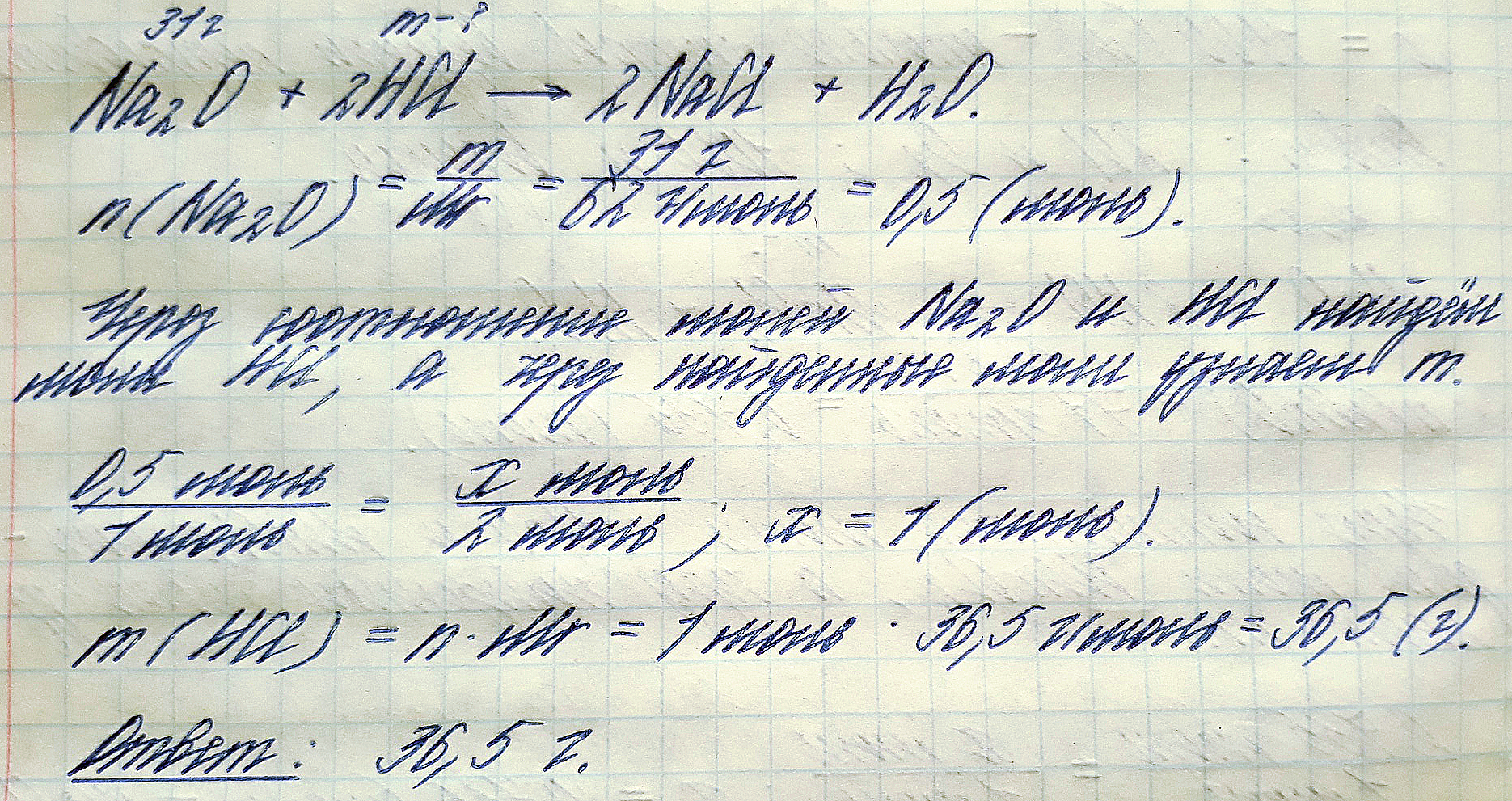
Ответ дал:
0
дано
m(Na2O) = 31 g
-------------------------
m(HCL)-?
Na2O+2HCL-->NaCL+H2O
M(Na2O) = 62 g/mol
n(Na2O) = m/M = 31 / 62 = 0.5 mol
n(Na2O) = 2n(HCL)
n(HCL) = 2*0.5 = 1 mol
M(HCL) = 36.5 g/mol
m(HCL) = n*M = 1*36.5 = 36.5 g
ответ 36.5 г
Приложения:
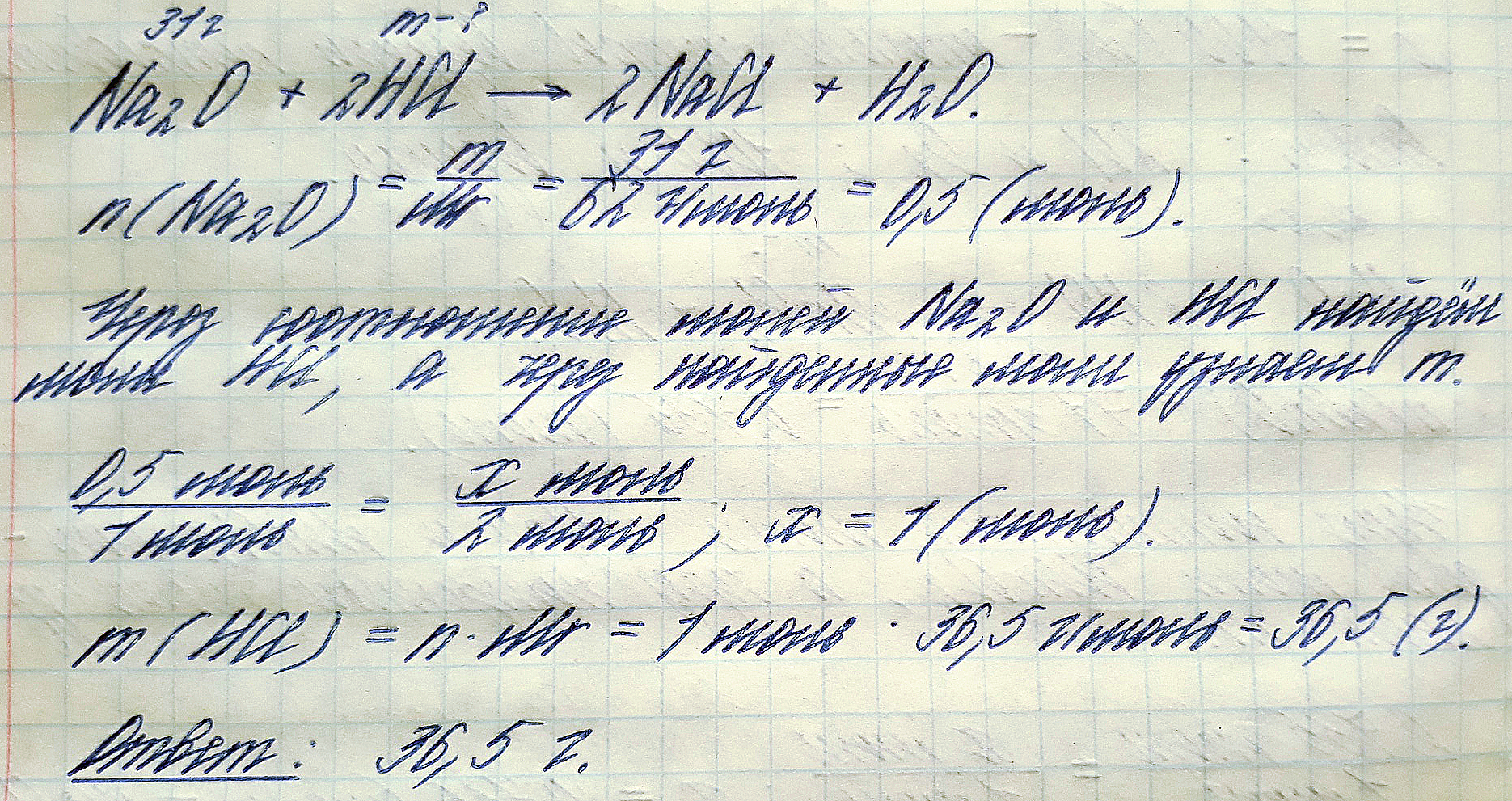
Вас заинтересует
2 года назад
3 года назад
3 года назад
9 лет назад
10 лет назад
10 лет назад