Сколько грамм осадка образуется при взаимодействии 160г. 10%-ного раствора сульфата меди (ll) с гидроксидом натрия
Ответы
Ответ дал:
0
Вот,лови решение всё подробно
Приложения:
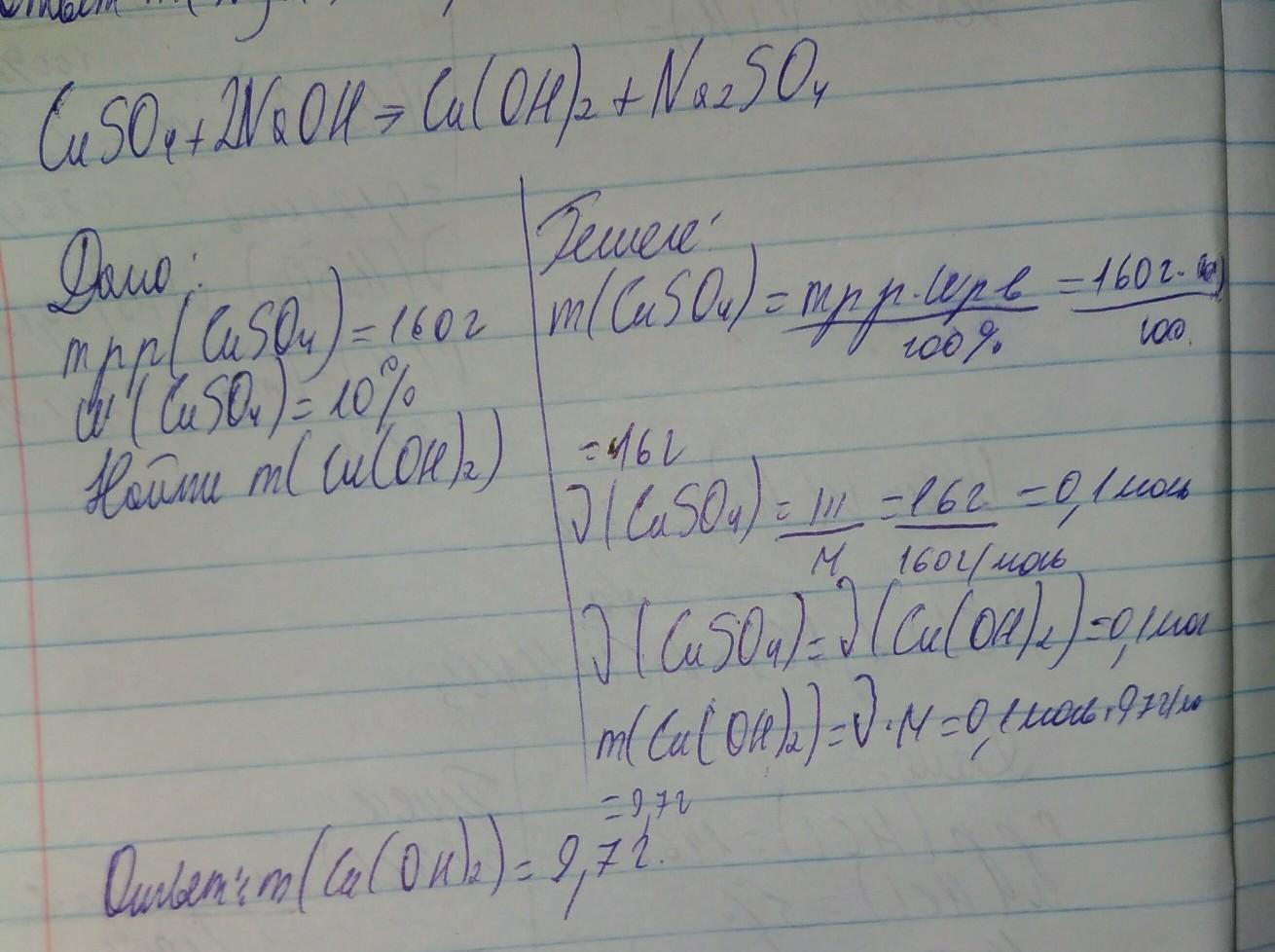
Ответ дал:
0
0,1 x
CuSO4+ 2NaOH = Na2SO4 + Cu(OH)2 Cu(OH)2 - осадок
1 1 0,1/1=х/1
m в(CuSO4)= 160 г * 0,1 = 16 г х= 0,1 моль (Cu(OH)2)
Mr (CuSO4) = 160 г/моль
n (CuSO4) = 16 г / 160 г/моль= 0,1 моль
Mr( Cu(OH)2) = 98 г/моль
m (Cu(OH)2)= 0,1 моль * 98 г/моль= 9,8 г
Приложения:
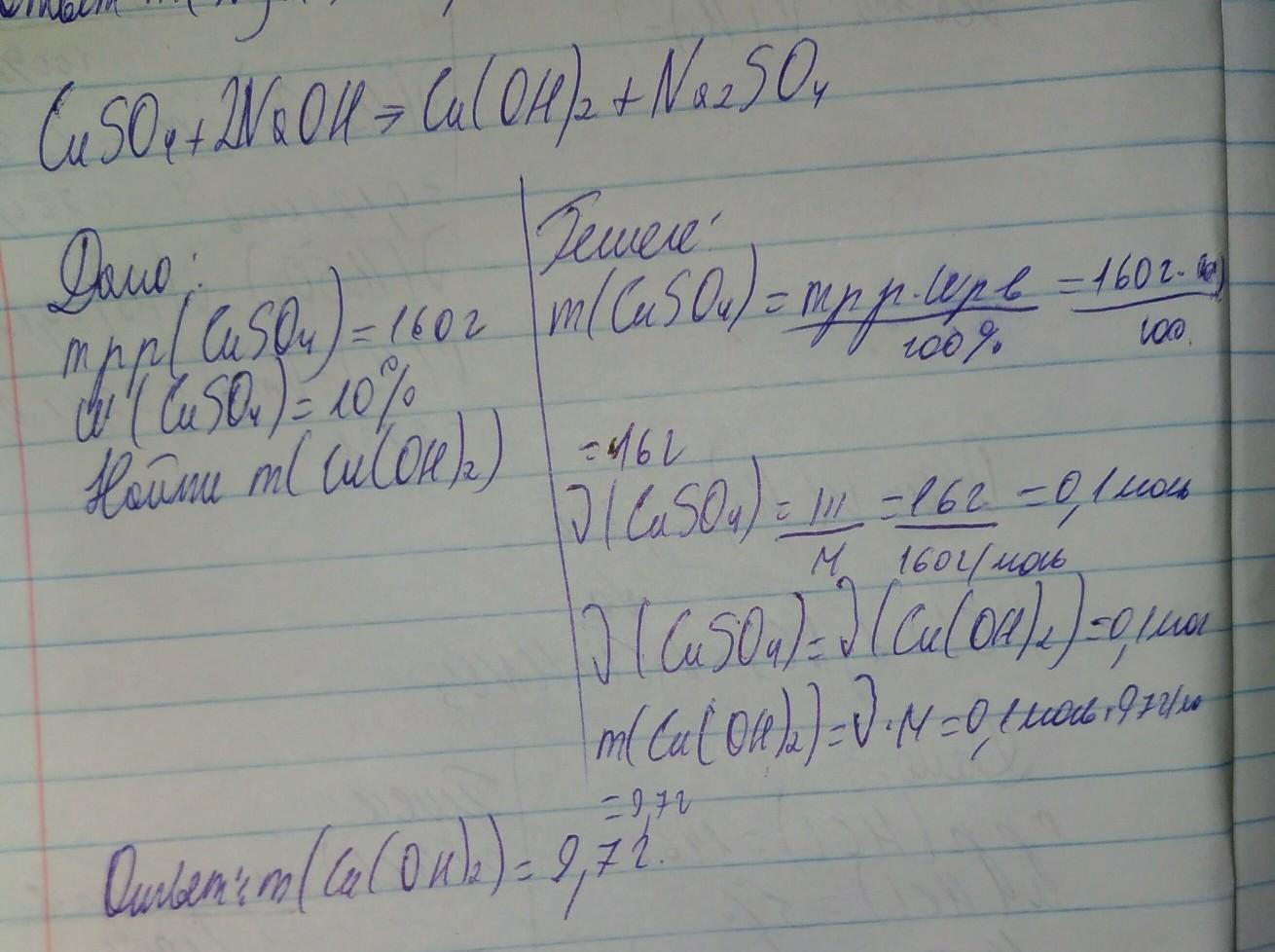
Вас заинтересует
2 года назад
3 года назад
3 года назад
9 лет назад
9 лет назад
10 лет назад