ПРОШУ ВАС УМОЛЯЮ МНЕ ЭТО ТОЖЕ НАДО РЕШИТЬ!!!! БЕЗУСЛОВНО 100 б.
как будет влиять увеличение температуры на состояние равновесия в следующих реакциях:
а) N + O2<=>2NO — Q
b) H2 + Cl2<=>2HCl + Q
Ответы
Ответ дал:
3
Увеличение температуры смещает равновесие в сторону эндотермической реакции.
А) Реакция эндотермическая, поглощение тепла. Равновесие сместится вправо. В сторону образования NO.
Б) Реакция экзотермическая, выделение тепла. Равновесие сместится влево. В сторону разложения HCl
Приложения:
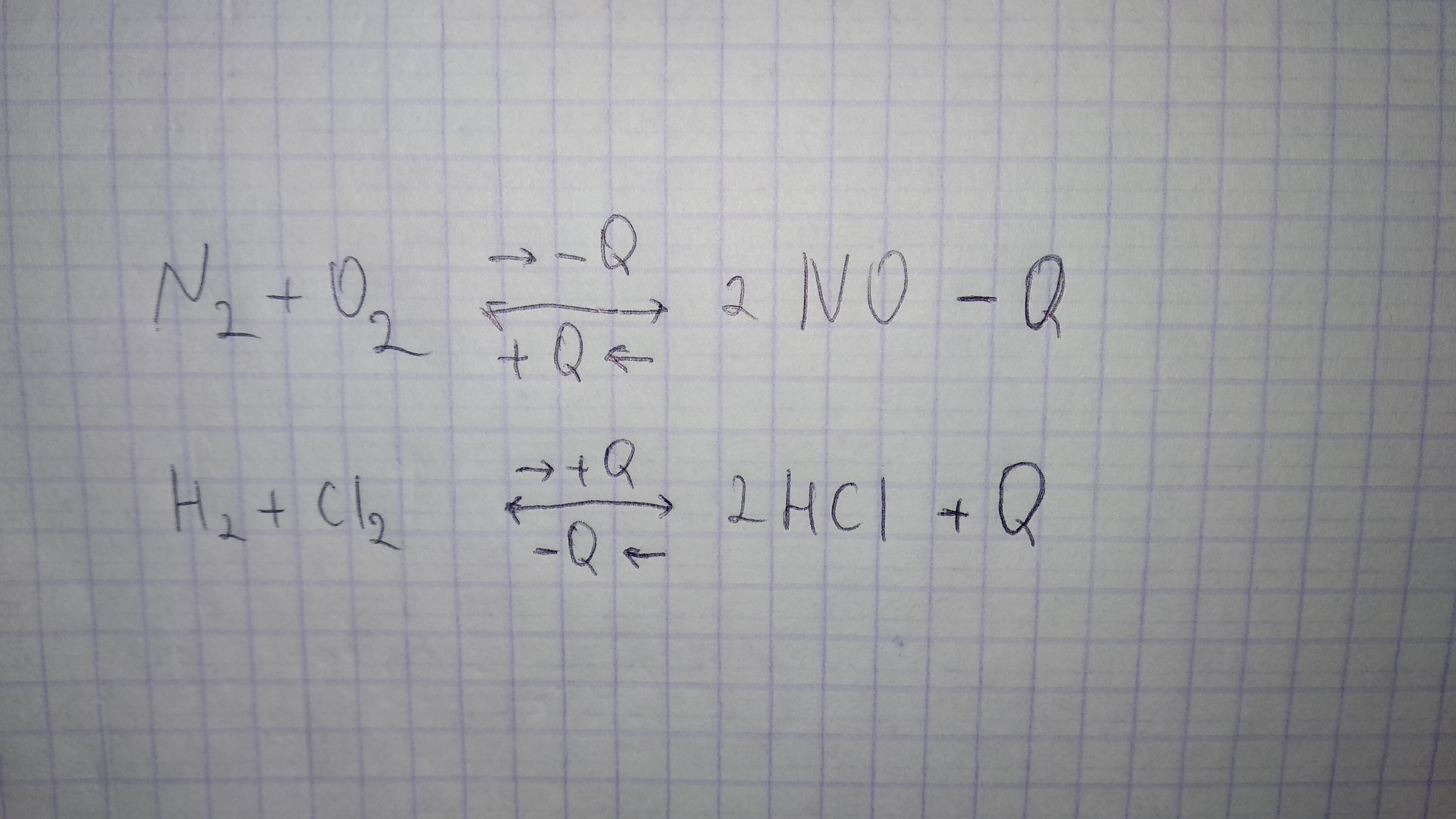
Turngait:
Только направление эндо- или экзотермического процесса
тогда получается вправо?
потому что реакция энотермическая и поголощает тепло
верно.
*?
Добавил фото. Разберётесь?
а что озночают стрелки?
с -Q и +Q
Это для пояснения. В какую сторону у данной реакции идёт эндотермической процесс, а в какую экзотермических. +Q это экзо, -Q это эндо. При повышении t реакция стремится в сторону эндопроцесса.
спасибо Вам
Вас заинтересует
2 года назад
2 года назад
2 года назад
2 года назад
3 года назад
9 лет назад