Кальций массой 0,8 г полностью растворили в избытке воды. Определите массу образовавшейся щелочи.
Ответы
Ответ дал:
0
Ответ:
Ca + 2H2O = Ca(OH)2 + H2
m (Ca) 0,8 г
m( Ca(OH)2) - ?
n = 0.8 г / 40 г/моль = 0.02 моль
n (Ca(OH)2)) = 0.02 моль
m ( (Ca(OH)2))) = 0.02 * 74 = 1,48 г
Объяснение:
Catofob:
А откуда появилось число 74 в конце?
ау
74 - молярная масса Ca(oh)2
Это молярная масса Сa(OH)2
Ответ дал:
0
Ответ: не уверена:)
Объяснение:
Приложения:
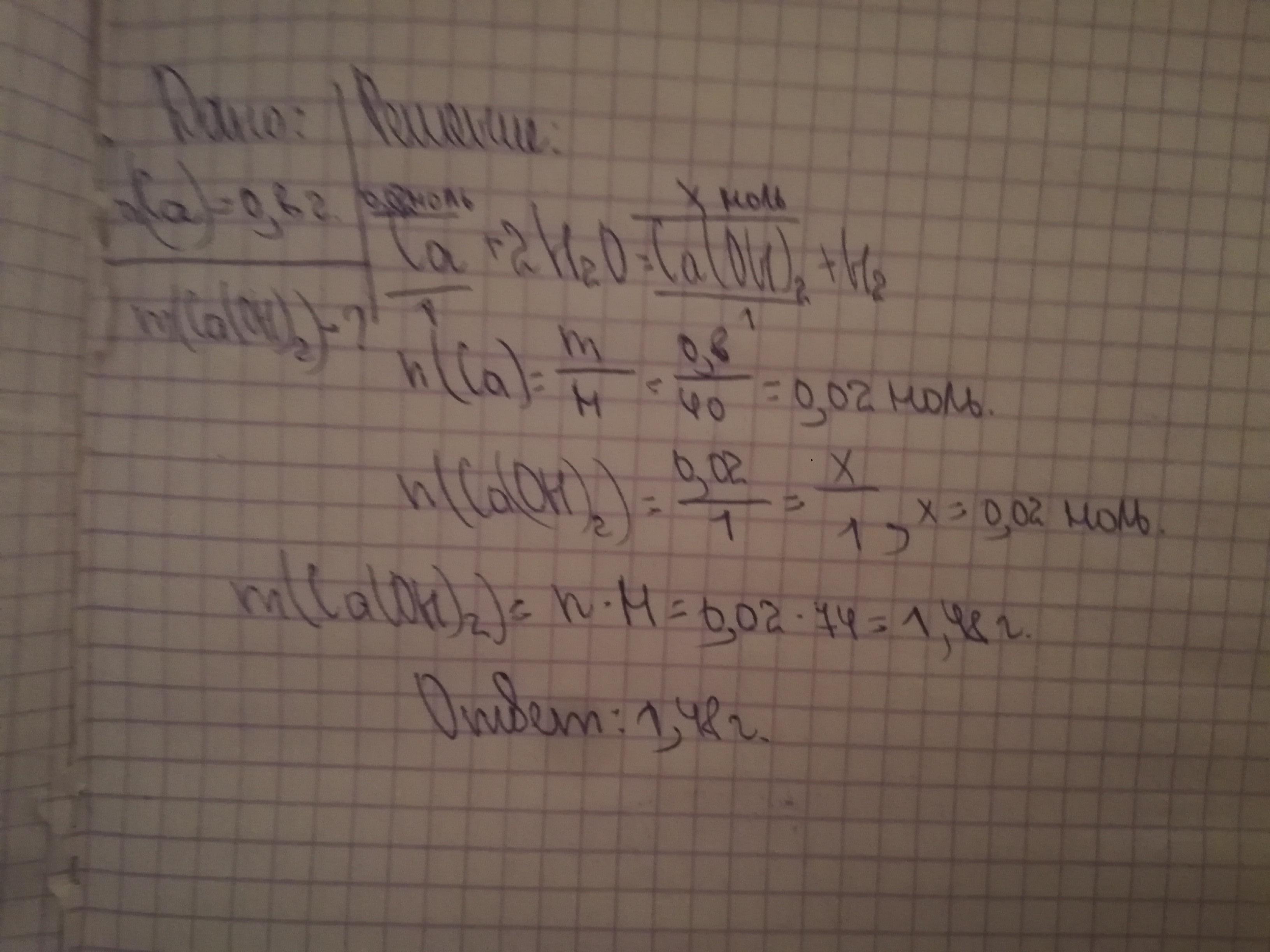
Вас заинтересует
2 года назад
2 года назад
2 года назад
2 года назад
3 года назад
3 года назад
9 лет назад