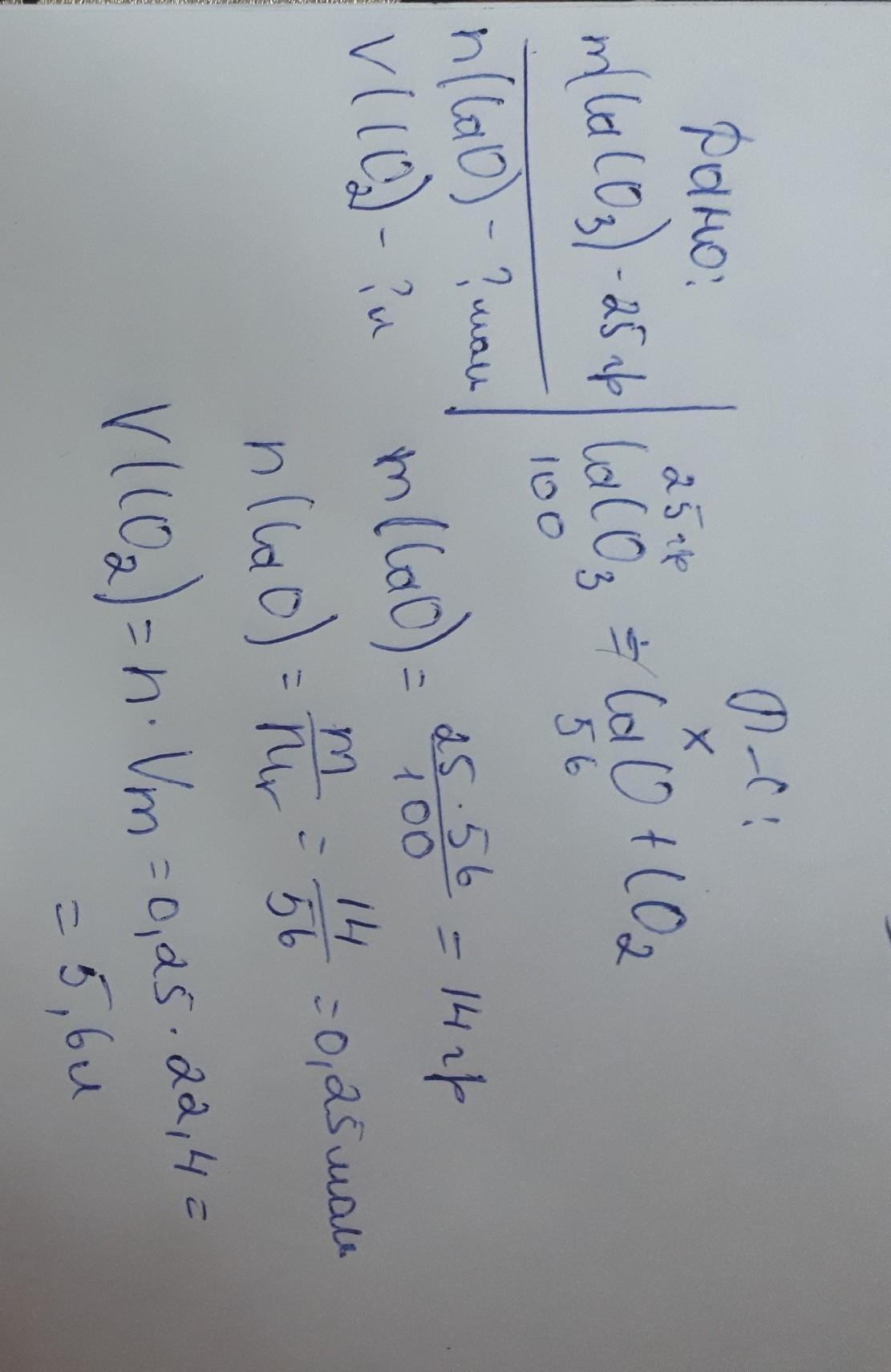Разложение карбоната кальция CaCO3, протекает
в соответствии с уравнением реакции
CaСО3= CaО + СО2. Какое количество
вещества оксида кальция Сао образуется при
разложении 25 г карбоната кальция? Какой
объем (н.у.) углекислого газа СО, при этом вы-
деляется?
Ответы
Объяснение:
n - кол-во вещества
V - объем
Что бы найти количество вещества, можно сделать пропорцию. 25Г надо поставить сверху CaCO3, а снизу его молярную массу, так как Если 25 / 100, то получится количество вещества, следовательно массу СаО, берем как Х, а молярную массу мы и можем найти благодаря таблице Менделеева. В результате,у нас получилась такая пропорция, 25 / 100 = Х/56. Так как X неизвестен, мы 56 умножаем на 25 и делим на 100. Благодаря этой пропорции, мы получаем массу СаО. Если, мы знаем массу, то мы можем найти "n".
Чтобы найти количество вещества, надо массу поделить на молярную массу (на фотографии показано решение). В результате чего получится, 0,25 моль.
В этой задаче, чтобы найти объем мы должны количество вещества умножить на Vm (Vm всегда равен 22.4 л). Количество вещества углекислого газа мы знаем, так как, Если количество вещества оксида кальция (СаО) равен 0,25 то и количество вещества углекислого газа (СО2) будeт равно 0,25, ведь реакция прошла полностью. Из-за этого мы спокойно можем выбрать количество вещества оксида кальция и для углекислого газа.
Надеюсь, я смогла объяснить.