помогите пж, срочно. Как решали тоже нужно!
Приложения:
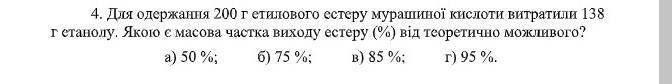
MilkyWay147:
если можно то напишите задачу на русском и я решу её. Это вроде по массовой доли растворов задача
Для получения 200г стилового эфира муравьиной кислоты потратили 138 г этанола. Какова массовая доля выхода эфира (%) от теоретически возможного?
Ответы
Ответ дал:
1
CHOOH + C2H5OH = CHOOC2H5 + H2O
Дано:
m(C2H5OH) - 128 г
m(CHOOC2H5) - 200г
Найти:
% выхода - ?
М(C2H5OH) = 46 г/моль
n(C2H5OH) = m/M = 138/46 = 3 моль
n(CHOOC2H5) = n (C2H5OH) = 3 моль (теоритически)
М(CHOOC2H5) = 74 г/моль
n(CHOOC2H5) = m/M = 200/74 = 2,7 моль (практически)
% выхода = 2,7 моль*100% / 3 моль = 90%
Ответ: 90%
Вас заинтересует
2 года назад
2 года назад
2 года назад
8 лет назад
8 лет назад
9 лет назад