Альдегід масою 2,15 г окисленили розчином аргентум оксиду, утворилось 5,4 г срібла. Визначте формулу альдегіду і відповідної кислоти
Ответы
Ответ дал:
7
Ответ:
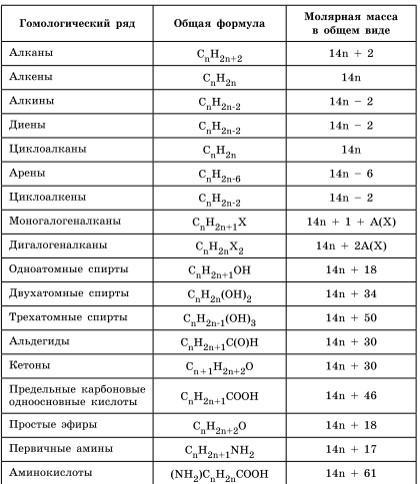
CnH2n+1C(O)H | 4 C4H9C(O)H
С4H9СOH - пентановый альдегид
Дано:
m( CnH2n+1C(O)H )=2,15г
m(Ag)=5,4г
Формула-?
-----------------------------------
2,15г 5,4г
CnH2n+1C(O)H+Ag2O->СnH2n+1-COOH+ 2Ag
14n+30 216г/моль
5,4(14n+30)=2,15*216
75,6n+162=464,4
75,6n=302,4
n=4
Приложения:
alinavegera46:
Откуда у тебя 216 г/моль взялось?
Объясни пожалуйста
Очень надо
2 моль серебра
1 моль это 108 г/моль, а 2 моль 216 г/моль
Спасибо большое!
)))
О я придумал нажми кнопку "Спасибо"
Вас заинтересует
2 года назад
2 года назад
3 года назад
3 года назад
8 лет назад
8 лет назад
9 лет назад