Определите, какая соль образуется при взаимодействии 24,52г серной
кислоты и 10г гидроксида натрия. Вычислите массу полученной соли.
Ответы
Ответ дал:
0
H2SO4 + 2NaOH --> Na2SO4 + 2H2O
n(H2SO4)=m/M = 24.52/98 = 0.25моль
n(NaOH) = 10/40 = 0.25 моль
n(Na2SO4) = n(NaOH) = 0.25 моль
m(Na2SO4) = M*n = 142 * 0.25 =35.5 г
n(H2SO4)=m/M = 24.52/98 = 0.25моль
n(NaOH) = 10/40 = 0.25 моль
n(Na2SO4) = n(NaOH) = 0.25 моль
m(Na2SO4) = M*n = 142 * 0.25 =35.5 г
Ответ дал:
0
надеюсь решение еще актуально)
Приложения:

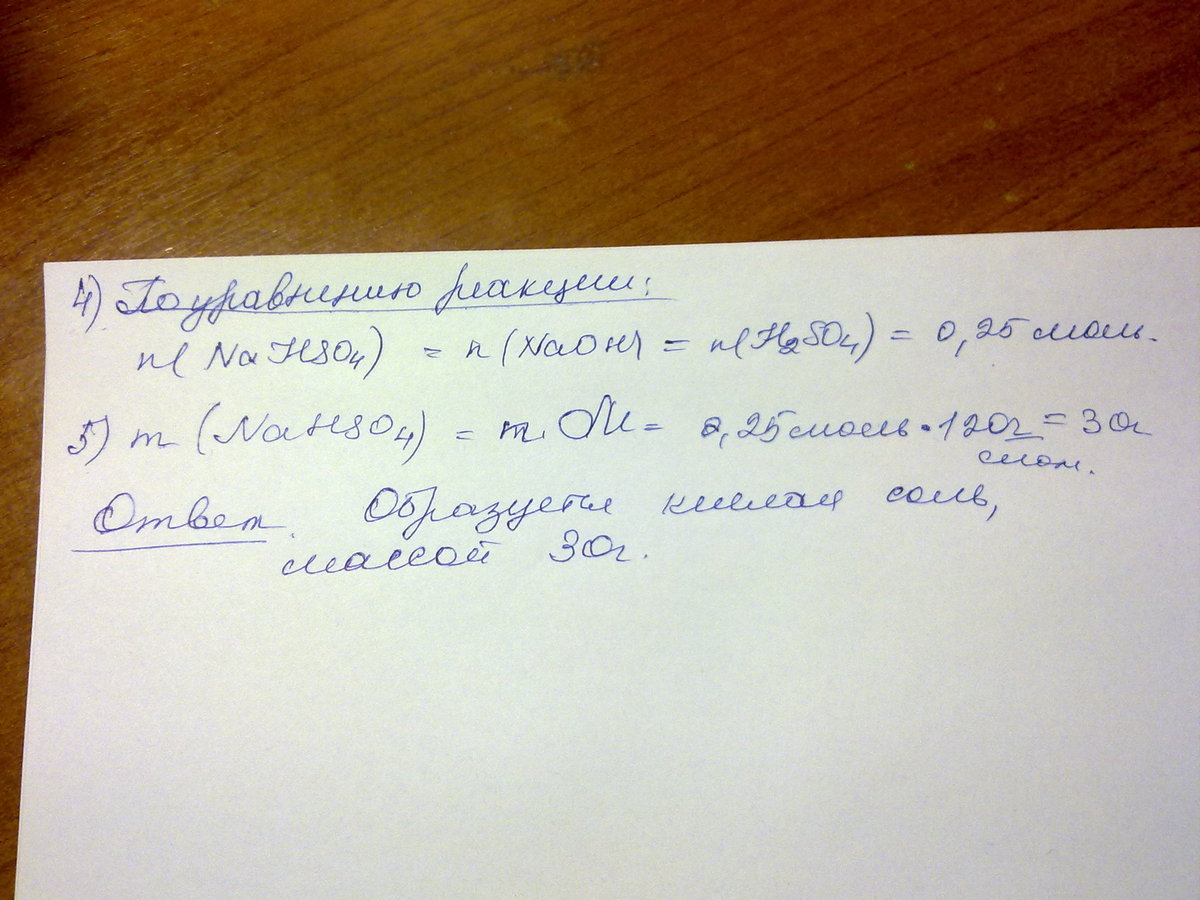
Вас заинтересует
3 года назад
3 года назад
8 лет назад
8 лет назад
11 лет назад
11 лет назад
11 лет назад
11 лет назад