Во сколько раз и как изменится скорость химической реакции при повышении температуры от 50 до 100 гр.цельсия, если температурный коэффициент равен 2.
Ответы
Ответ дал:
0
увеличится в 32 раза
V2/V1=K2/K1=u^(T2-T1)/10
(T2-T1)/10=100-50/10=5
u=2
V2/V1=2^5=2*2*2*2*2=32
V2/V1=K2/K1=u^(T2-T1)/10
(T2-T1)/10=100-50/10=5
u=2
V2/V1=2^5=2*2*2*2*2=32
Ответ дал:
0
а можно полностью расписать, пожалуйста)))
Ответ дал:
0
Решение смотри во вложениях.
Приложения:
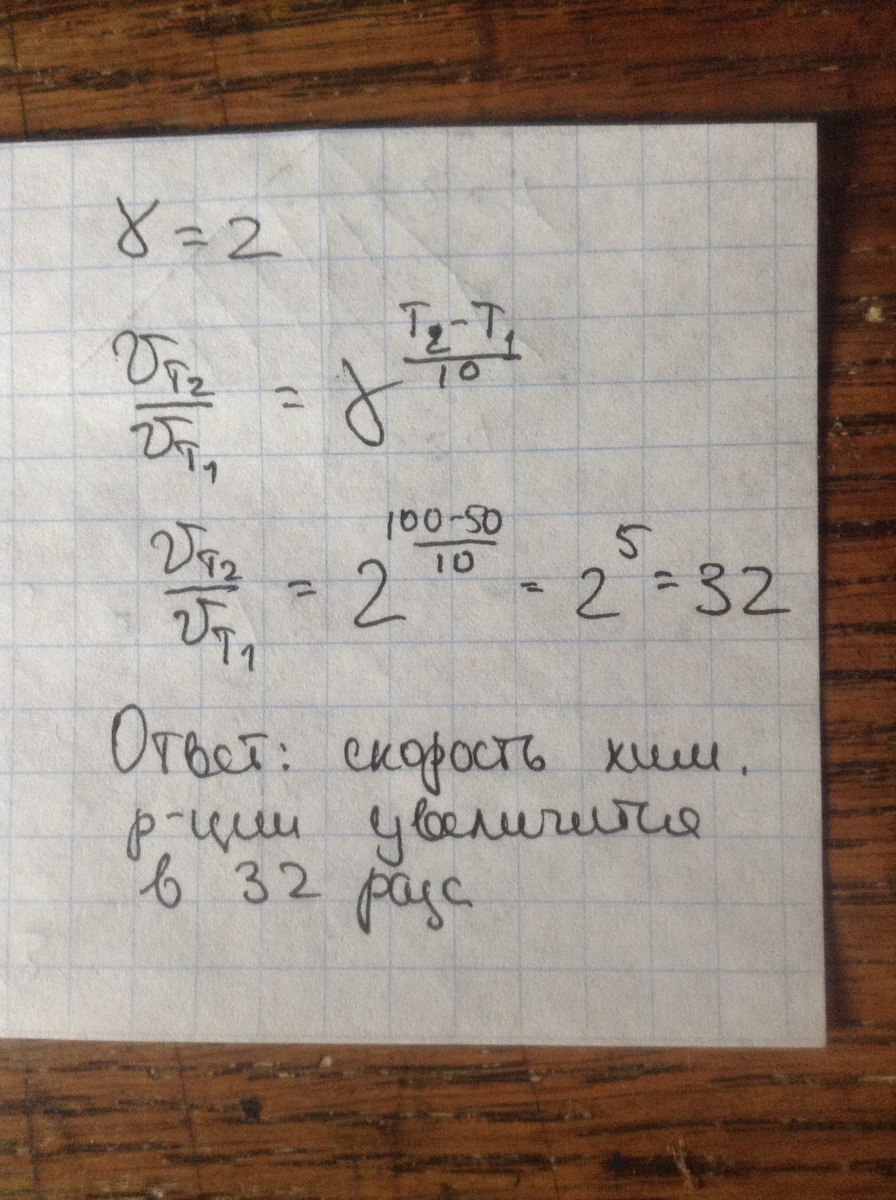
Вас заинтересует
3 года назад
3 года назад
8 лет назад
11 лет назад
11 лет назад