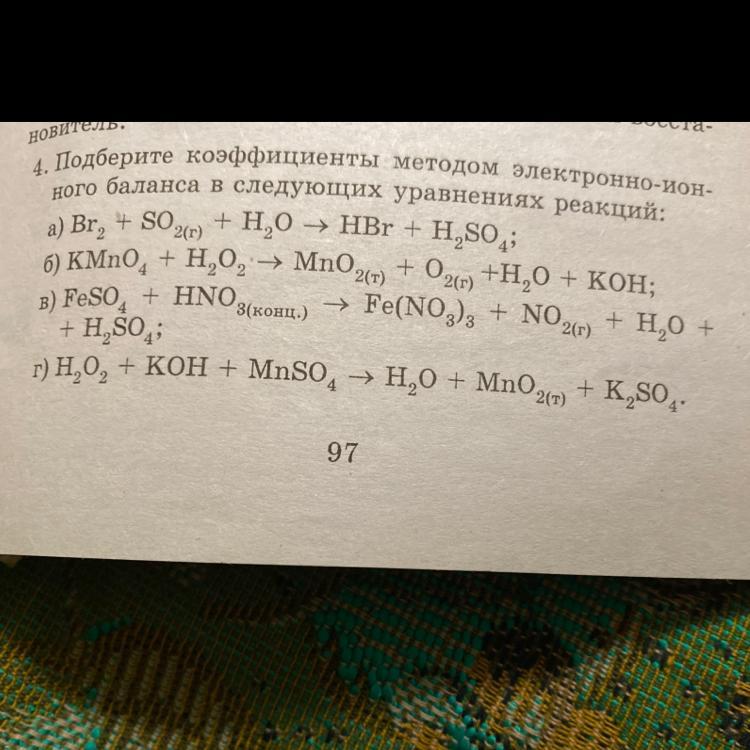Ответы
Ответ дал:
0
Ответ:
а) Br2 + SO2 + 2H2O = 2HBr + H2SO4
Br2(0) +1e*2 = 2Br(-) 2 1 - восстановление
S(+4) -2e = S(+6) 2 1 - окисление
Br2 - окислитель (Br2(0))
SO2-восстановитель (S(+6))
б) 2KMnO4+3H2O2=2MnO2+2H2O+2KOH
Mn(+7) +3e=Mn(+4) 2 -окислитель
2O(-1) -2e=O2(0) 3-восстановитель
в) Fe⁺²SO₄ + 4HN⁺⁵O₃(конц.) =Fe⁺³(NO₃)₃ + N⁺⁴O₂(г) + H₂O + H₂SO₄
Fe⁺² - e⁻ = Fe⁺³ | 1 восстановитель, процесс окисления
N⁺⁵ + e⁻ = N⁺⁴ | 1 окислитель, процесс восстановления
г)H₂O₂⁻ +KOH +Mn⁺²SO₄ --> H₂O⁻² +Mn⁺⁴O₂ +K₂SO₄
Mn⁺² -2e = Mn⁺⁴ 1 - восстановитель, окисляется, окисление
2
O₂⁻ +2e = 2O⁻² 1 - окислитель, восстанавливается, восстановление
Fufelman777:
Это электронный баланс,краткий вариант овр. А нужен метод полуреакций,который определяет среду.
Так бы в вопросе и написал, чтобы понятней было.
Вас заинтересует
2 года назад
2 года назад
3 года назад
3 года назад
8 лет назад
8 лет назад
10 лет назад
10 лет назад