Ответы
Ответ дал:
1
Объяснение:
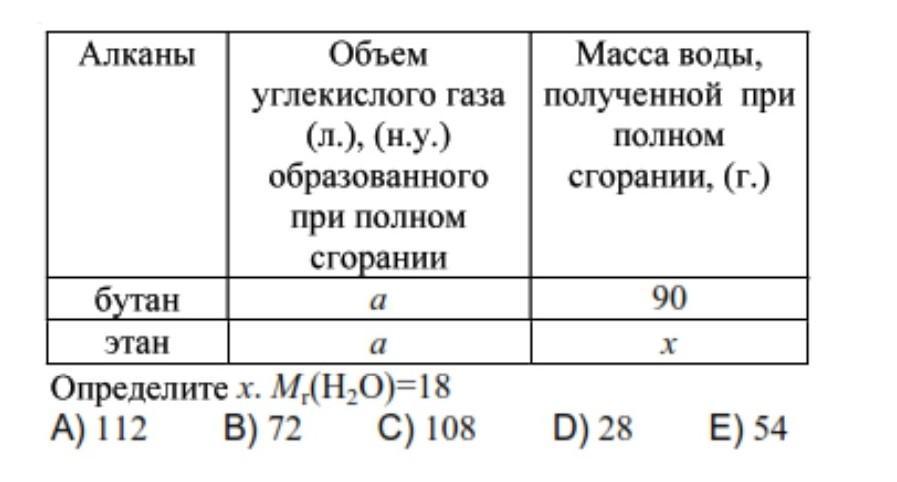
2C4H10 + 13O2 = 8CO2 + 10H2O
n(H2O)=m÷M=90÷(10×18)=0.5моль
2C2H6 + 7O2 → 4CO2 + 6Н20
m=n×M=0.5×6×18=54г
Раз объёмы одинаковы, то при сгорании этана образовалось 4 моль СО2, значит этана было взято 4/2 = 2 моль;
При сгорании 2 моль этана образуется 6*2/2 = 6 моль воды.
Объёмы газов должны быть равны.Их можно уровнять, если поделить коэффициенты в уравнении горении бутана на 2
Не забывай про доп. условие - массу воды.
Делать можно, что угодно, в соотв. условием.
Нашла и поняла ошибку.
Знать бы как ее исправить((((
2C4H10 + 13O2 = 8CO2 + 10H2O
n(H2O)=m÷M=90÷(10×18)=0.5моль
2C2H6 + 7O2 → 4CO2 + 6Н20
m=n×M=0.5×6×18=54г
n(H2O)=m÷M=90÷(10×18)=0.5моль
2C2H6 + 7O2 → 4CO2 + 6Н20
m=n×M=0.5×6×18=54г
2C4H10 + 13O2 = 8CO2 + 10H2O
n(H2O)=m÷M=90÷(10×18)=0.5моль n(CO2)=
8×5÷10=4 моль 2C2H6 + 7O2 → 4CO2 + 6Н20
m=n×M=(4×6×18)÷4=108г
n(H2O)=m÷M=90÷(10×18)=0.5моль n(CO2)=
8×5÷10=4 моль 2C2H6 + 7O2 → 4CO2 + 6Н20
m=n×M=(4×6×18)÷4=108г
Спасибо Всем Онромное
Вас заинтересует
2 года назад
2 года назад
3 года назад
3 года назад
9 лет назад
10 лет назад