Какой объем раствора с массовой долей гидроксида калий 15% (плотность 1,13 г/мл)
необходим для нейтрализации этановой кислоты количеством вещества 0,6 моль?
Ответы
Ответ дал:
1
Ответ:
198,23 мл
Объяснение:
СH3COOH + KOH = CH3COOK + H2O
n(KOH)=n(CH3COOH)=0.6 моль
m(KOH)=0.6*56=33,6 грамм
m(KOH 15%)=33.6/0.15=224 грамма
V(KOH)=224/1.13=198,23 мл
zvetochok:
А почему n(KOH)=n(CH3COOH)?
Согласно реакции. Эквиваленты у них равны одноосновная кислота и одноосновной гидрооксид.
Аа,точно, это с пропорции можно узнать, спасибо большое :)
Ответ дал:
0
Ответ:
ответ на фото можно лучший ответ плзззззззззззззззз
Приложения:
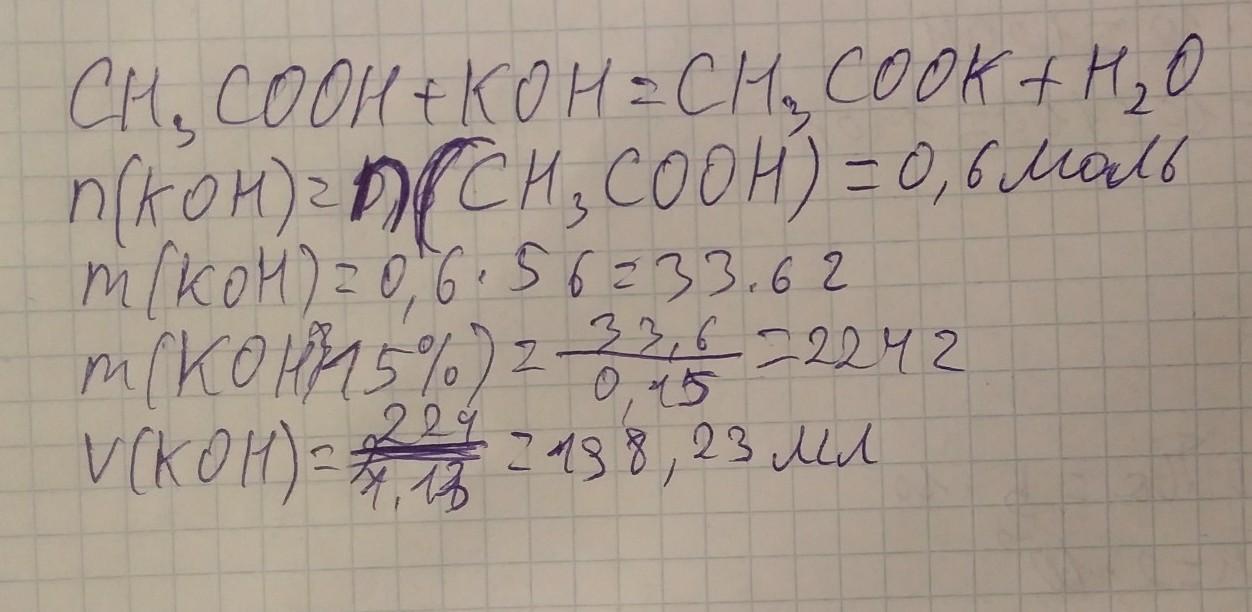
Вас заинтересует
2 года назад
2 года назад
3 года назад
3 года назад
8 лет назад
8 лет назад
10 лет назад