Кальций массой 30 г обработали соляной кислотой. Далее образованный водород использовали для получения аммиака. Найдите объем азота, который вступил в реакцию и объем полученного аммиака. (если выход продукта 15%).
Ответы
Ответ дал:
0
Удачи!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
Приложения:
Ответ дал:
1
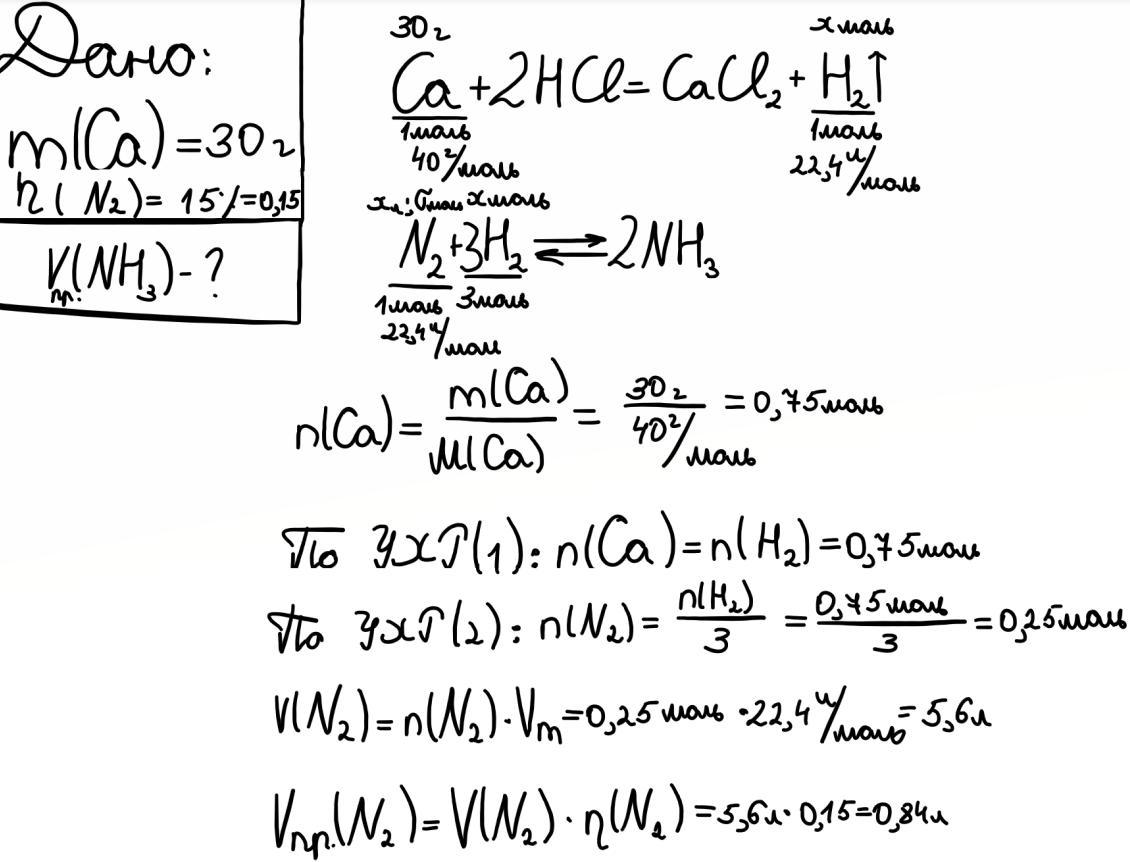
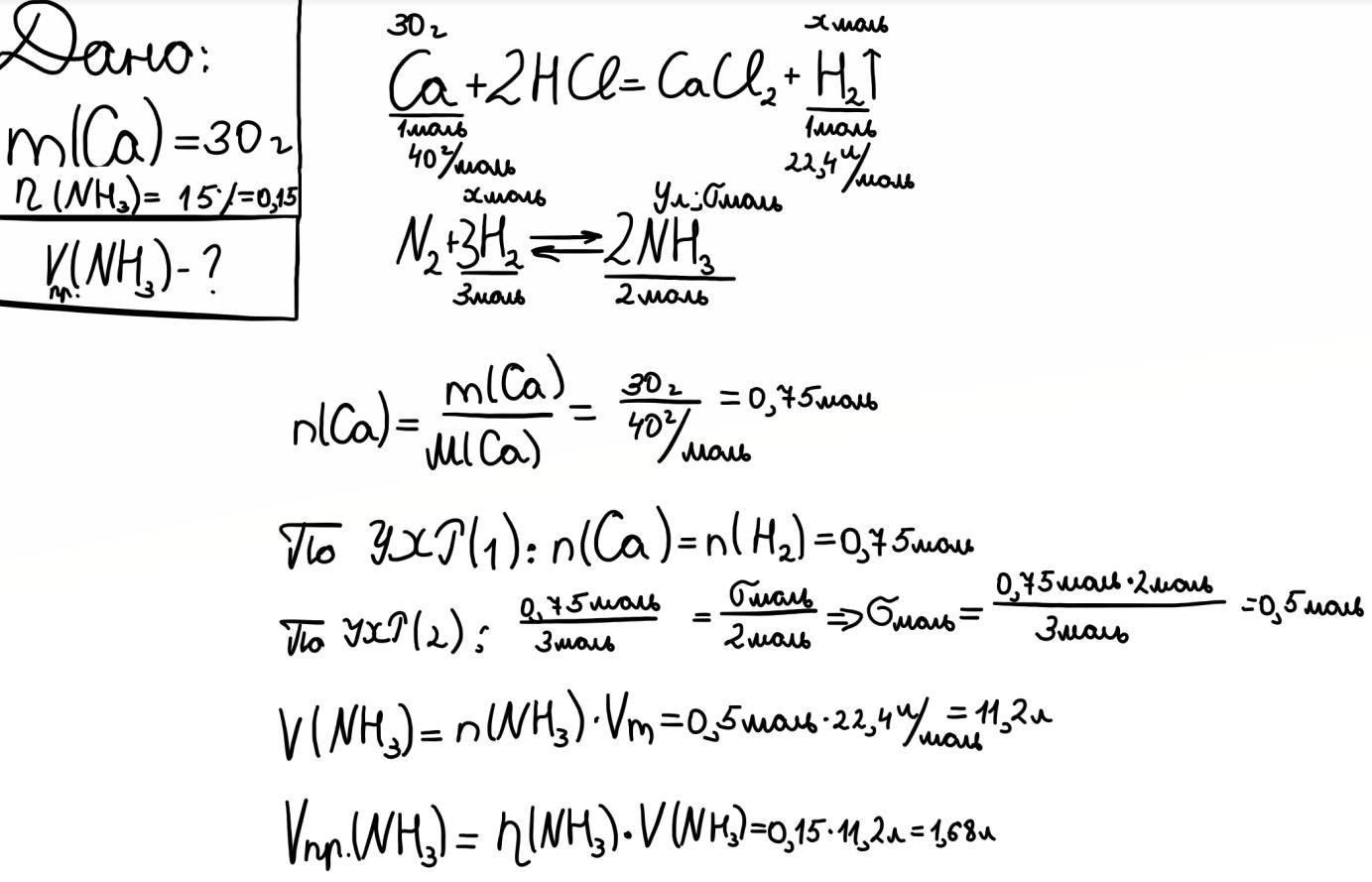
Дано:
m(Ca) = 30 г
η(NH3) = 15%
Найти:
V(N2) - ?
V практ.(NH3) - ?
Решение:
1) Ca + 2HCl → CaCl2 + H2;
3H2 + N2 → 2NH3;
2) n(Ca) = m / M = 30 / 40 = 0,75 моль;
3) n(H2) = n(Ca) = 0,75 моль;
4) n(N2) = n(H2) / 3 = 0,75 / 3 = 0,25 моль;
5) V(N2) = n(N2) * Vm = 0,25 * 22,4 = 5,6 л;
6) V теор.(NH3) = V(N2) * 2 = 5,6 * 2 = 11,2 л;
7) V практ.(NH3) = η * V теор. / 100% = 15% * 11,2 / 100% = 1,68 л.
Ответ: Объем N2 составляет 5,6 л; практический NH3 - 1,68 л.
Вас заинтересует
1 год назад
1 год назад
1 год назад
3 года назад
3 года назад
8 лет назад
8 лет назад