ПРОШУ ОЧЕНЬ НУЖЕН ОТВЕТ!
Вычислите объем водорода, который выделится при взаимодействии 183,6 г алюминия с избытком соляной кислоты.
Ответ дайте в литрах с точностью до десятых
Ответы
Ответ дал:
0
Удачи!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
Приложения:
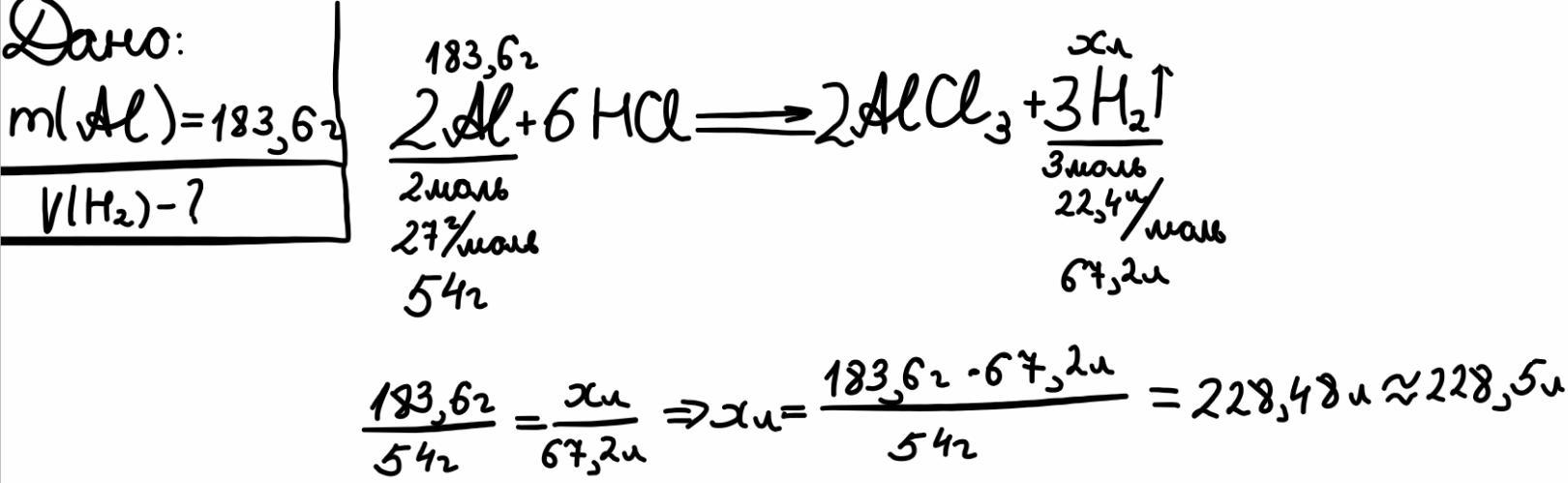
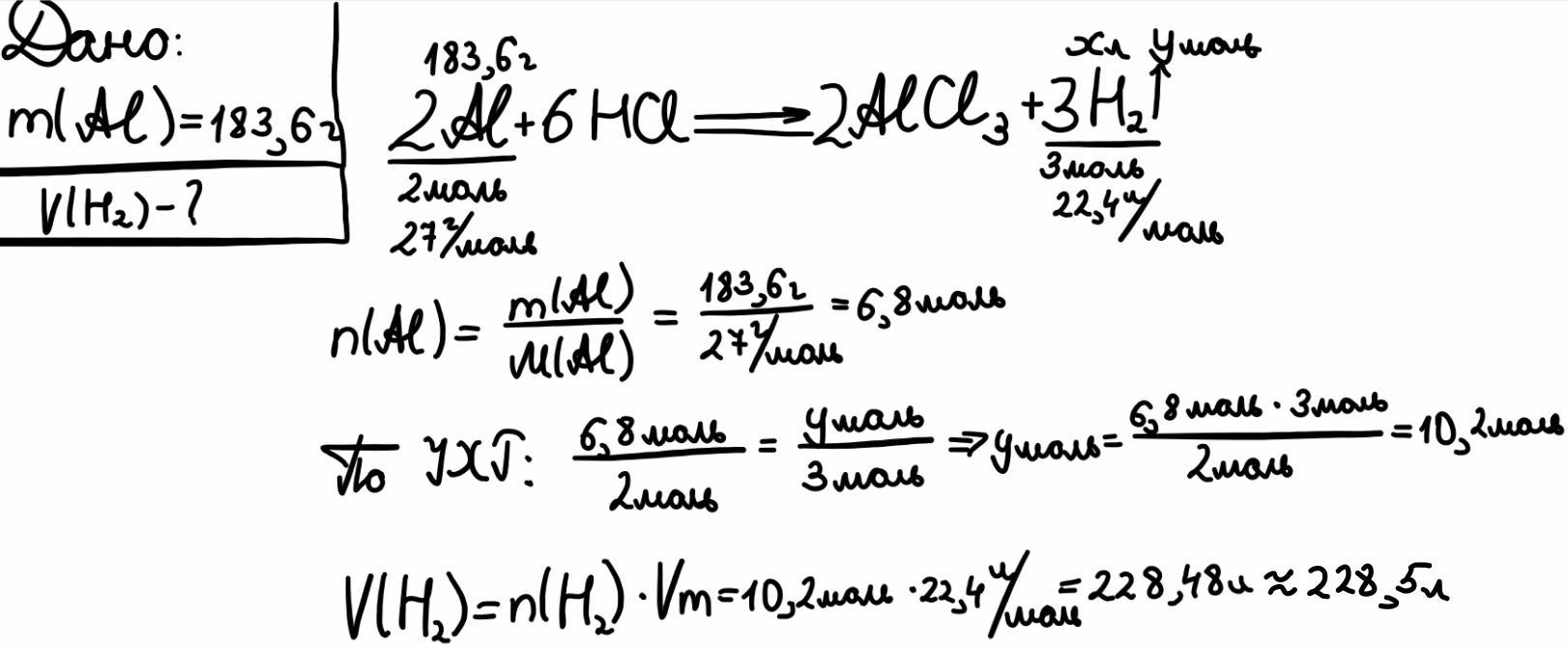
Ответ дал:
0
Дано:
m(Al) = 183,6 г
Найти:
V(H2) - ?
Решение:
1) 2Al + 6HCl → 2AlCl3 + 3H2↑;
2) n(Al) = m / M = 183,6 / 27 = 6,8 моль;
3) n(H2) = n(Al) * 3 / 2 = 6,8 * 3 / 2 = 10,2 моль;
4) V(H2) = n(H2) * Vm = 10,2 * 22,4 = 228,48 ≈ 228,5 л.
Ответ: Объем H2 составляет 228,5 л.
Вас заинтересует
1 год назад
2 года назад
2 года назад
3 года назад
3 года назад
8 лет назад