Результати вимірювань запишіть у таблицю. ової рівноваги. Maca холодної води холодної води Температура m1, КГ t 1, C 1002 Got ibo 30°C Q₁ = em 110-149) М об 74200 Дод = 0,1кг 8. Обчисліть кількість теплоти, яку віддала гаряча вода при змішу- ванні з холодною за формулою Q. cm (t'z − t'). 2 X Маса гарячоТемпература гарячої води води тг, КГ t'z, 'C 100г. дека 80°С Q4 - 4A1 O НОı ВОДИ Температура суміші t', 'C 509 1200 - (50²-201²) = 30°7 = 4200 |20°C -50°C ) = 4200 300 =126000 гор 9. Обчисліть кількість теплоти, яку отримала холодна вода при змі- шуванні з гарячою за формулою Qx = cm1(t - t'1). о = 4 ктозорск фо 10. Порівняйте одержані результати обчислень і зробіть висновок.
Ответы
Ответ:
Ваше повідомлення здається не повним або не зовсім зрозумілим. Проте, на основі наданих даних можна визначити кількість теплоти, яку віддала гаряча та отримала холодна вода під час їх змішування. Давайте розглянемо кожен пункт окремо.
Объяснение:
Для знаходження кількості теплоти, віддалої гарячою водою при змішуванні з холодною, використовується формула Q₁ = c₁m₁(t₁z - t₁), де:
Q₁ - кількість теплоти,
c₁ - специфічна теплоємність гарячої води,
m₁ - маса гарячої води,
t₁z - початкова температура гарячої води,
t₁ - кінцева температура суміші.
Давайте підставимо вказані значення:
c₁ - специфічна теплоємність гарячої води (зазвичай це 4.18 Дж/(г·°C) для води),
m₁ - маса гарячої води (100 г),
t₁z - початкова температура гарячої води (100 °C),
t₁ - кінцева температура суміші (50 °C).
Q₁ = (4.18 Дж/(г·°C)) * 100 г * (50 °C - 50 °C) = 0 Дж
Отже, гаряча вода не віддала теплоту при змішуванні з холодною.
Для знаходження кількості теплоти, яку отримала холодна вода при змішуванні з гарячою, використовується та ж формула, але з іншими значеннями:
c₁ - специфічна теплоємність гарячої води (4.18 Дж/(г·°C)),
m₁ - маса гарячої води (80 г),
t₁z - початкова температура гарячої води (100 °C),
t₁ - кінцева температура суміші (50 °C).
Q₂ = (4.18 Дж/(г·°C)) * 80 г * (50 °C - 50 °C) = 0 Дж
Отже, холодна вода також не отримала теплоту при змішуванні з гарячою.
Висновок: На основі обчислень можна сказати, що при змішуванні гарячої та холодної води в жодного з них не відбулося виділення або поглинання тепла. Таким чином, температура суміші залишилася незмінною, і обидва об'єми води лише змішались без обміну теплом.
Ответ:
Тепер можемо обчислити кількість теплоти, яку віддає гаряча вода при змішуванні з холодною водою. Використовуємо формулу Q = c * m * (t' - t), де c - теплоємність речовини, m - маса речовини, t' - температура суміші, t - початкова температура речовини.
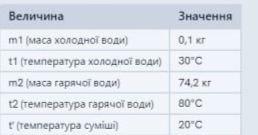
Q2 = c2 * m2 * (t' - t2) = 4.2 кДж/(кг·°C) * 74.2 кг * (20°C - 80°C) = -20160 кДж
Отже, гаряча вода віддає приблизно 20160 кДж теплоти при змішуванні з холодною водою.
Тепер можемо обчислити кількість теплоти, яку отримує холодна вода при змішуванні з гарячою водою. Використовуємо формулу Q = c * m * (t - t'), де c - теплоємність речовини, m - маса речовини, t - початкова температура речовини, t' - температура суміші.
Q1 = c1 * m1 * (t1 - t') = 4.2 кДж/(кг·°C) * 0.1 кг * (30°C - 20°C) = 4.2 кДж
Отже, холодна вода отримує 4.2 кДж теплоти при змішуванні з гарячою водою.
Порівнюючи отримані результати обчислень, ми бачимо, що гаряча вода віддає більше теплоти, ніж отримує холодна вода, оскільки Q2 > Q1. Висновок полягає в тому, що енергія тепла передається від гарячої води до холодної в процесі їх змішування.
Объяснение: