помогите пожалуйста
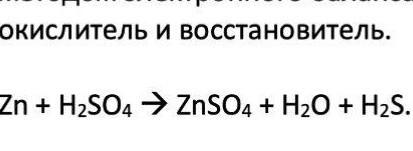
определите степень окисления всех элементов, расставьте коэффициенты методом электронного баланса, определите окислитель и восстановитель
Приложения:
Ответы
Ответ дал:
1
H2so4 окислитель, Zn восстановитель
Приложения:
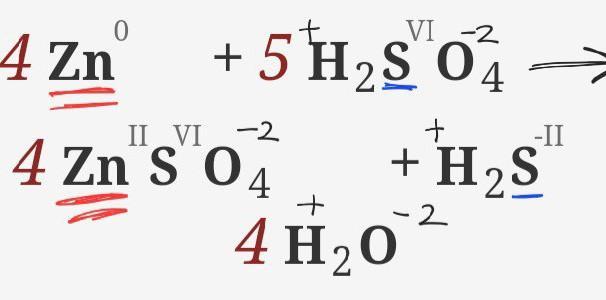

Ответ дал:
0
Відповідь:
Уравнение : Zn + H2SO4 → ZnSO4 + H2S + H2O
Расставляем коэфициенты:
общее число электронов, отданных восстановителем, должно быть равно общему числу электронов, принятых окислителем.
4 Zn⁰ + 5 H2S⁶O4 → 4 Zn²S⁶O4 + H2S⁻² + 4 H2O
Это окислительно-восстановительная (редокс) реакция:
S(VI) + 8 e- → S()-II (восстановление)
4 Zn(0) - 8 e- → 4 Zn (II) (окисление)
H2SO4 является окислителем, Zn является восстановителем.
Определяем степени окисления всех елементов в соединениях
4.Определяем степени окисления всех елементов в соединениях:
4 Zn + 5 H2SO4→ 4 ZnSO4 + H2S + 4 H2O
Zn (0)
+1+6 -2
H2 SO4
I VI -II
+2 +6 -2
Zn S O4
II VI -II
+1 -2
H2 S
I -II
+1 -2
H2 O
I -II
Пояснення:
Вас заинтересует
2 года назад
2 года назад
2 года назад
3 года назад
3 года назад
8 лет назад
8 лет назад