В 50г 7%-го раствора серной кислоты поместили цинк,массой 6.5.Найти объем выделившегося водорода
Ответы
Ответ дал:
0
H2SO4+Zn----->ZnSO4+H2;
mв-ва(H2SO4)=50*0,07=3,5г
n(Zn)=6,5/65=0,1моль(избыток)
n(H2SO4)=3,5/98=0,04моль(недостаток)
Расчет ведем по недостатку!
n(H2SO4)=n(H2)=0,04моль
V(H2)=0,04*22,4=0,896л
Ответ дал:
0
реш.влож.
.....................
Приложения:
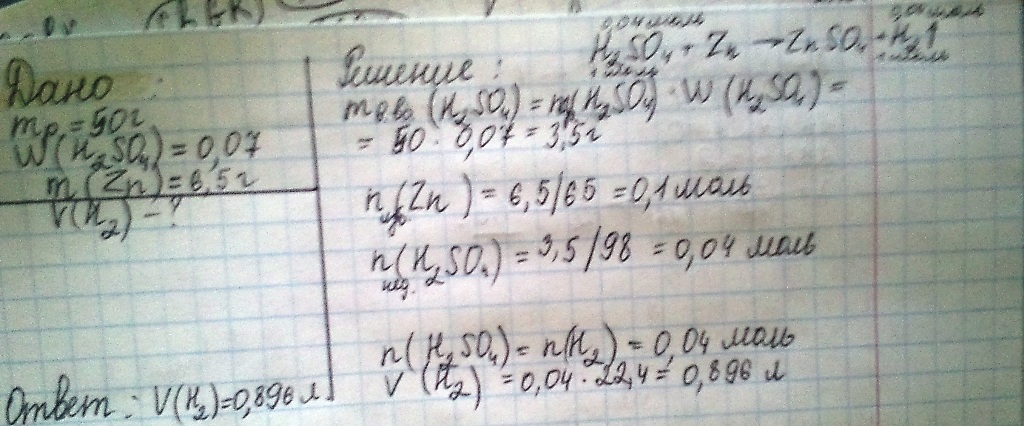
Вас заинтересует
3 года назад
8 лет назад
11 лет назад
11 лет назад