Определите степени окисления HCl в след кислотах:
1) HClO, HClO2, HClO3, HClO4. Напишите формулы соответствующие этим кислотным оксидам.
2) Составьте графические формулы фосфорной, угольной и серной кислот.
3) Напишите уравнения реакций характиризующая способы получения и химические свойства гидрооксида алюминия
Ответы
Ответ дал:
0
Будет вот так. А с гидроксидом алюминия распиши, что взаимодействует с кислотами, со щелочами, образуя комплексные соединения.
Приложения:
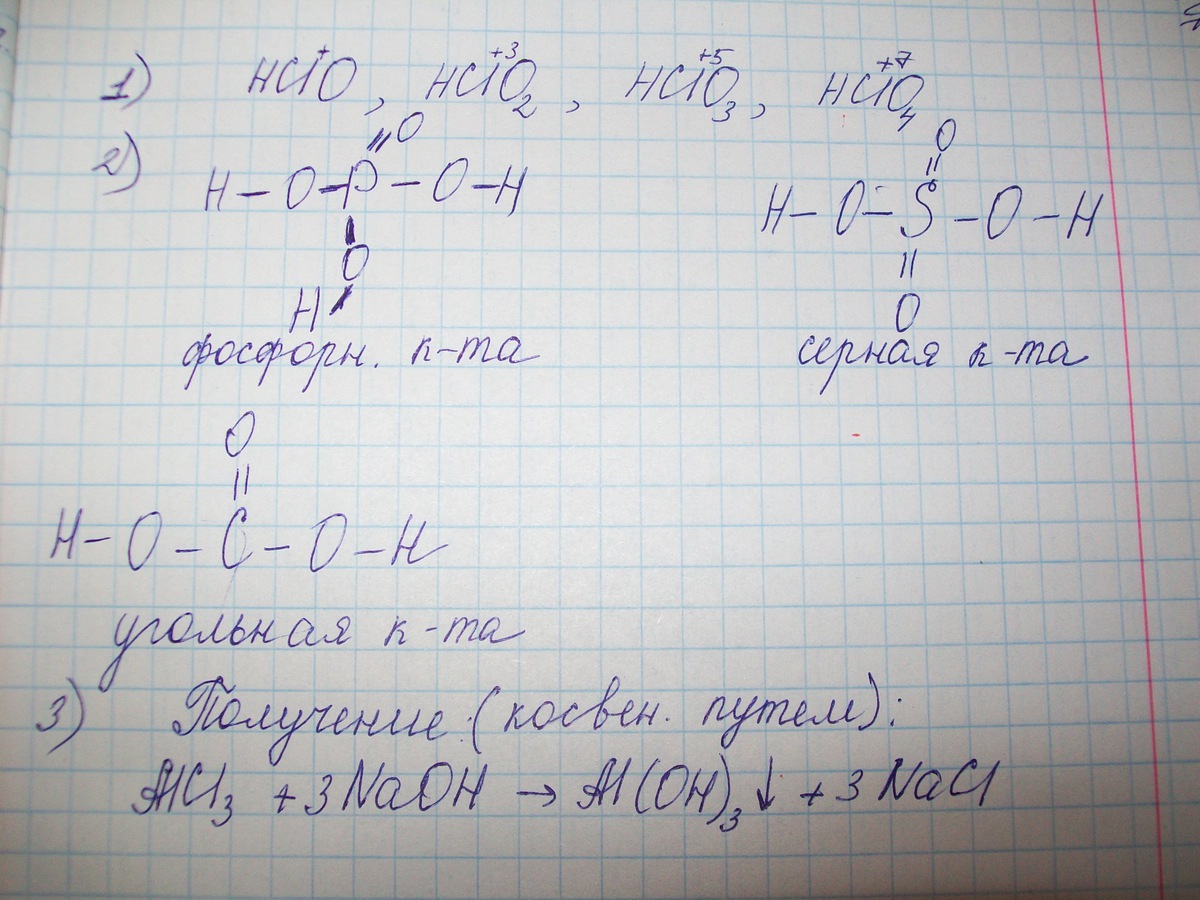
Ответ дал:
0
hclo хлорноватистая кислота ее соль naclo гипохлорит натрия
hclo2 хлористая кислота naclo2 ее соль хлорит натрия
hclo3 хлорноватая кислота ее соль kclo3 хлорат калия она же бертолетовая соль
hclo4 хлорная кислота ее соль kclo4 перхлорат калия
2 структурные формулы можно составить самому если знаешь Валентность элементов.. так у фосфора 5 углерода 4 у серы 6 она численно равно номеру группы в таблице менделеева..
гидроксид алюминия это осадок белого цвета поэтому его получают реакцией обмена например
alcl3+3naoh=3nacl+al(oh)3
albr3+3koh=3kbr+al(oh)3
al2o3+3h2o=2al(oh)3
гидроксид алюминия амфотерный следовательно он будет реагировать с и с кислотами и с щелочами например
2al(oh)3+3h2so4=al2(so4)3+6h2o
или например с соляной кислотой
al(oh)3+3hcl=alcl3+3h2o
al(oh)3+naoh=na[al(oh)4] комплексное соединение тетрагидроксоалюминат натрия или с
al(oh)3+koh=k[al(oh)4] тетрагидроксоалюминат калия
алюминий используется в алюмотермии
fe2o3+al=fe+al2o3 из реакции видно что железо получили в 'чистом' виде..
hclo2 хлористая кислота naclo2 ее соль хлорит натрия
hclo3 хлорноватая кислота ее соль kclo3 хлорат калия она же бертолетовая соль
hclo4 хлорная кислота ее соль kclo4 перхлорат калия
2 структурные формулы можно составить самому если знаешь Валентность элементов.. так у фосфора 5 углерода 4 у серы 6 она численно равно номеру группы в таблице менделеева..
гидроксид алюминия это осадок белого цвета поэтому его получают реакцией обмена например
alcl3+3naoh=3nacl+al(oh)3
albr3+3koh=3kbr+al(oh)3
al2o3+3h2o=2al(oh)3
гидроксид алюминия амфотерный следовательно он будет реагировать с и с кислотами и с щелочами например
2al(oh)3+3h2so4=al2(so4)3+6h2o
или например с соляной кислотой
al(oh)3+3hcl=alcl3+3h2o
al(oh)3+naoh=na[al(oh)4] комплексное соединение тетрагидроксоалюминат натрия или с
al(oh)3+koh=k[al(oh)4] тетрагидроксоалюминат калия
алюминий используется в алюмотермии
fe2o3+al=fe+al2o3 из реакции видно что железо получили в 'чистом' виде..
Приложения:
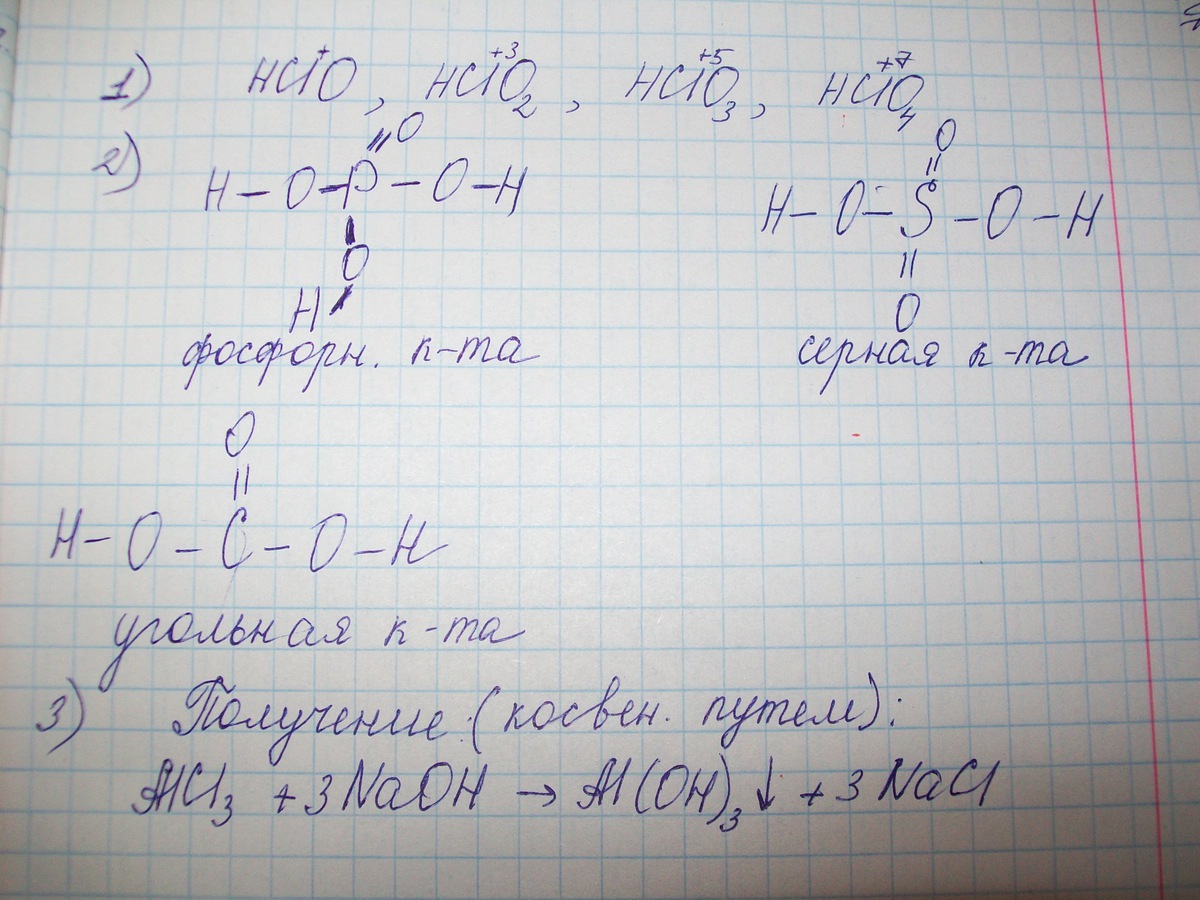
Ответ дал:
0
дополнение к первому пункту: кислотные окисды:
Вас заинтересует
3 года назад
3 года назад
8 лет назад
11 лет назад
11 лет назад
11 лет назад