Ответы
Ответ дал:
0
............................
Приложения:
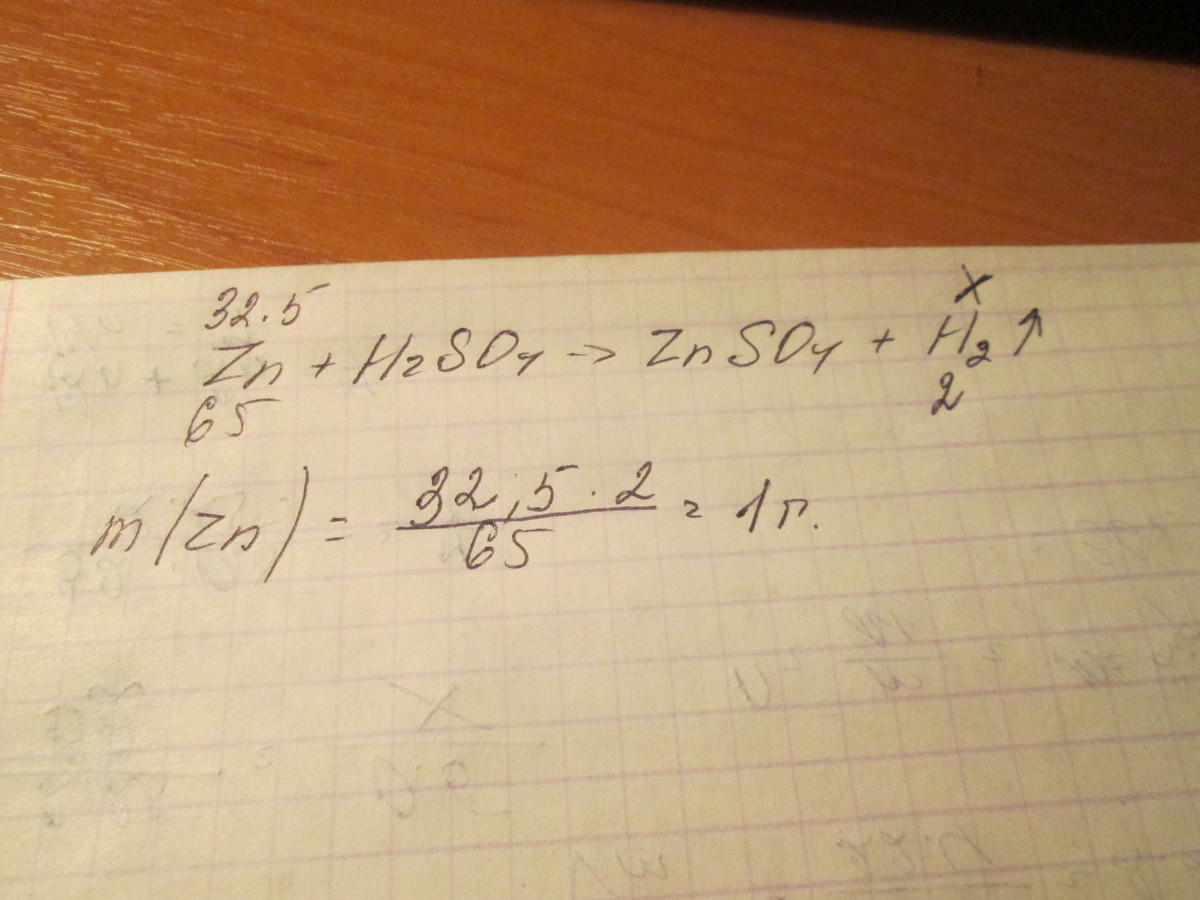
Ответ дал:
0
Спасибо большое )))))
Ответ дал:
0
Zn+H2SO4=ZnSO4+H2
Сначала находим малярную массу цинка, и следовательно у водорода будет та же самая малярная масса:
V(Zn)=32.5г/(65г/моль)=0.5моль
Теперь находим массу водорода(H2):
m(H2)=0.5моль*(2г/моль)=1 г
Ответ: 1г
Если что-то не понятно, спроси объясню.
Приложения:
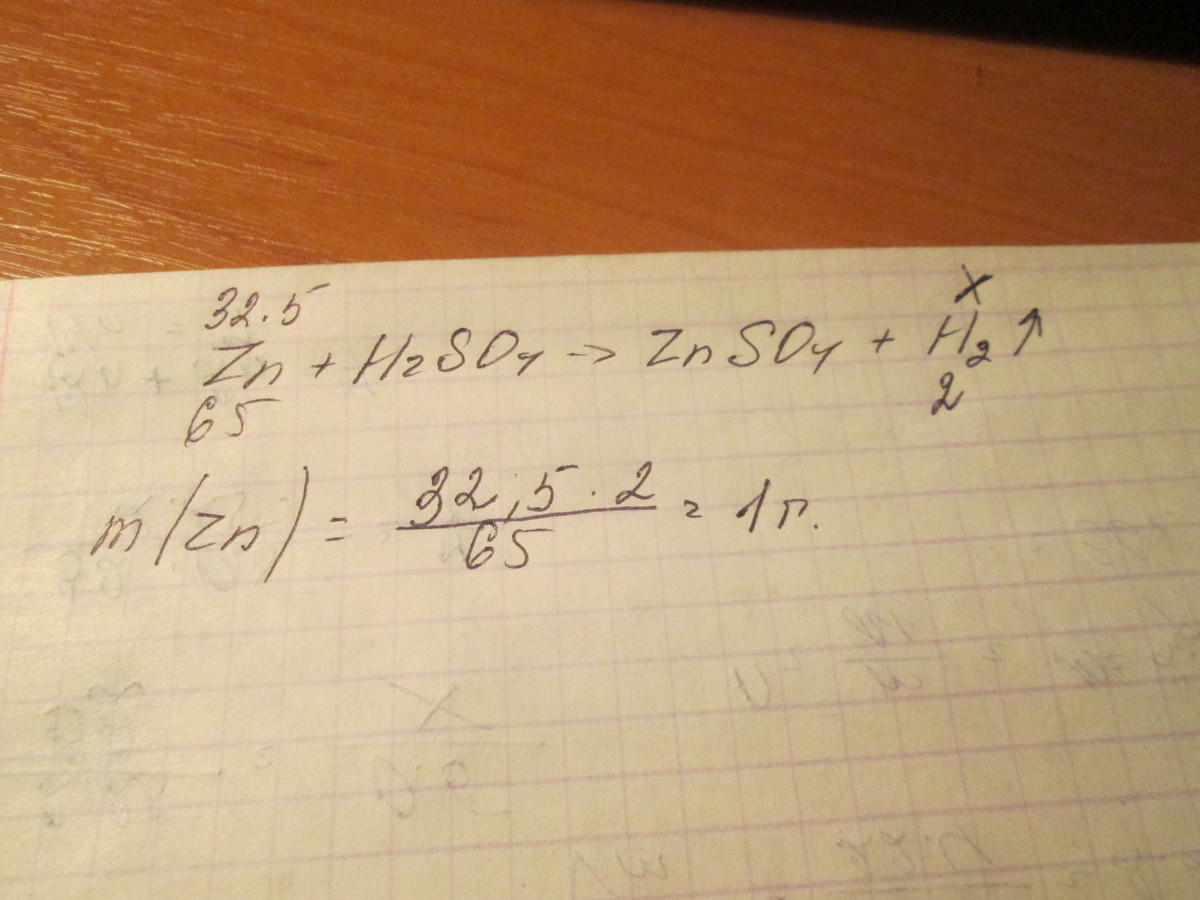
Вас заинтересует
3 года назад
3 года назад
8 лет назад
10 лет назад
11 лет назад