Некоторый элемент проявляет в оксиде степень окисления +4. Массовая доля этого элемента в оксиде составляет 71,17%. Какой это элемент? Напишите формулу оксида. (Se)
ПОМОГИТЕ ОЧЕНЬ СРОЧНО!
Ответы
Ответ дал:
0
Молярная масса этого оксида равна
M(XO2) = x + 32
w(X) = x/(x+32) *100% = 71.17%
Решим это уравнение:
х/(х+32) = 0.7117
0.2883 х = 22.77
х=78.98 г/моль
Смотрим в таблицу Менделеева - это селен Se
M(XO2) = x + 32
w(X) = x/(x+32) *100% = 71.17%
Решим это уравнение:
х/(х+32) = 0.7117
0.2883 х = 22.77
х=78.98 г/моль
Смотрим в таблицу Менделеева - это селен Se
Приложения:
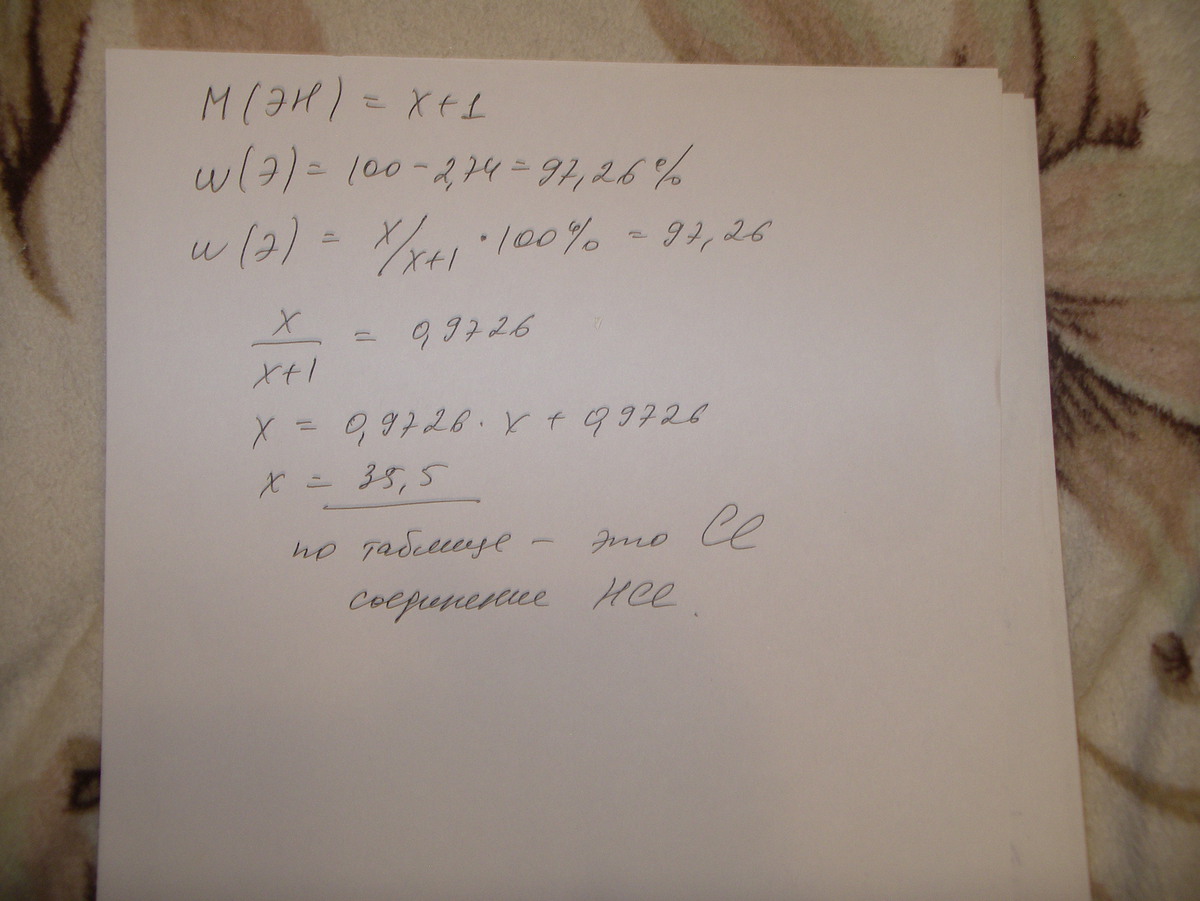
Ответ дал:
0
привет ты можешь мне решить по химии ещё 3 задания, ну и всё
Ответ дал:
0
ну пожалуйста только ты был бы в сети молю прям как Бога тебя
Ответ дал:
0
ну прошу
Ответ дал:
0
:):):):):) :)))))
Ответ дал:
0
да, я здесь
Ответ дал:
0
Запишем общую формулу оксида неизвестного элемента ЭО2
На долю кислорода в этом оксиде приходится 100%-71,17%=28,83% по массе
Масса атомов кислорода в оксиде 16*2=32
Находим массу неизвестного элемента из пропорции
28,83% - 32
71,17% - х
х= 71,17*32/28,83 = 78,9
Смотрим в таблицу - это селен.
Формула оксида SeO2
На долю кислорода в этом оксиде приходится 100%-71,17%=28,83% по массе
Масса атомов кислорода в оксиде 16*2=32
Находим массу неизвестного элемента из пропорции
28,83% - 32
71,17% - х
х= 71,17*32/28,83 = 78,9
Смотрим в таблицу - это селен.
Формула оксида SeO2
Приложения:
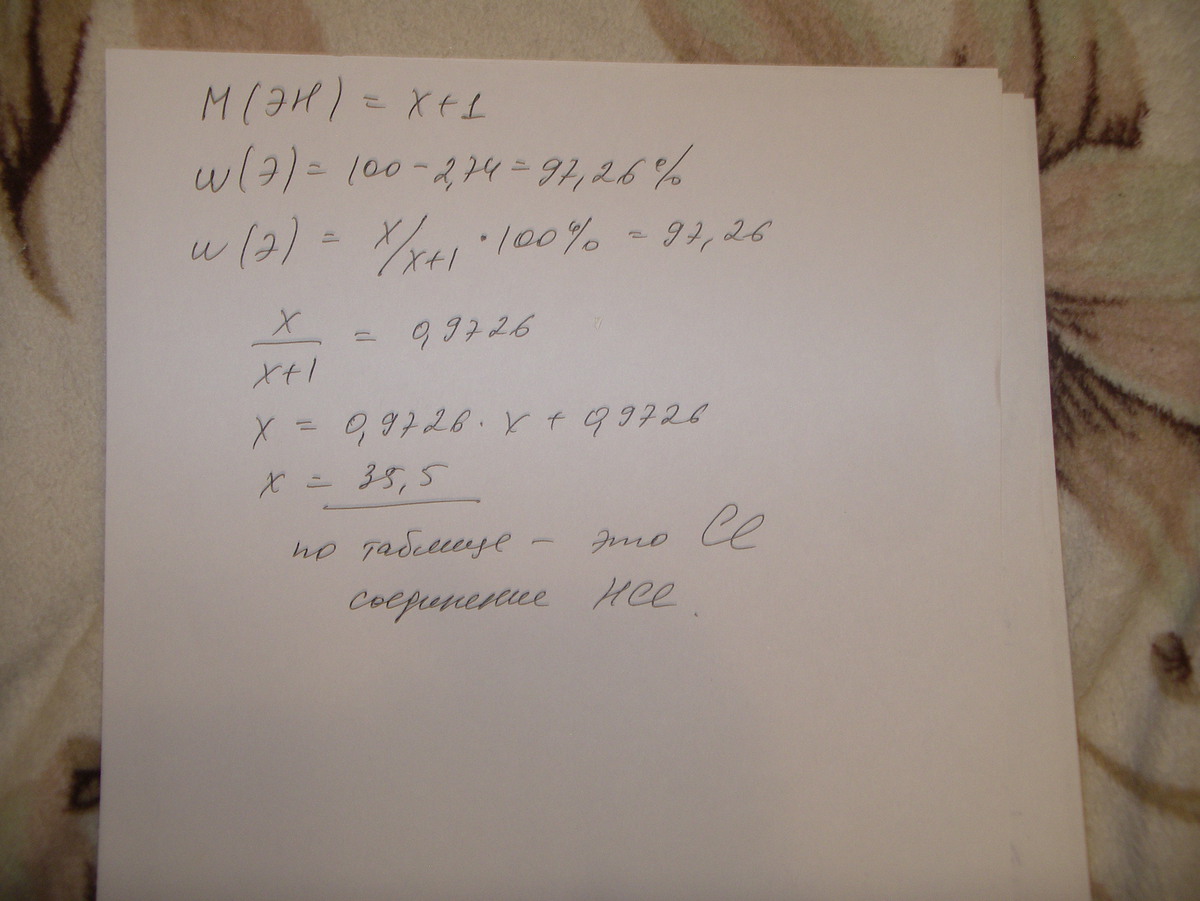
Вас заинтересует
3 года назад
3 года назад
8 лет назад
10 лет назад
10 лет назад
11 лет назад