Определите избыточное вещество и массу этого вещества при реакции взаимодействия 4,6 г натрия c 5,4 г воды
Ответы
Ответ дал:
1
Удачи!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
Приложения:
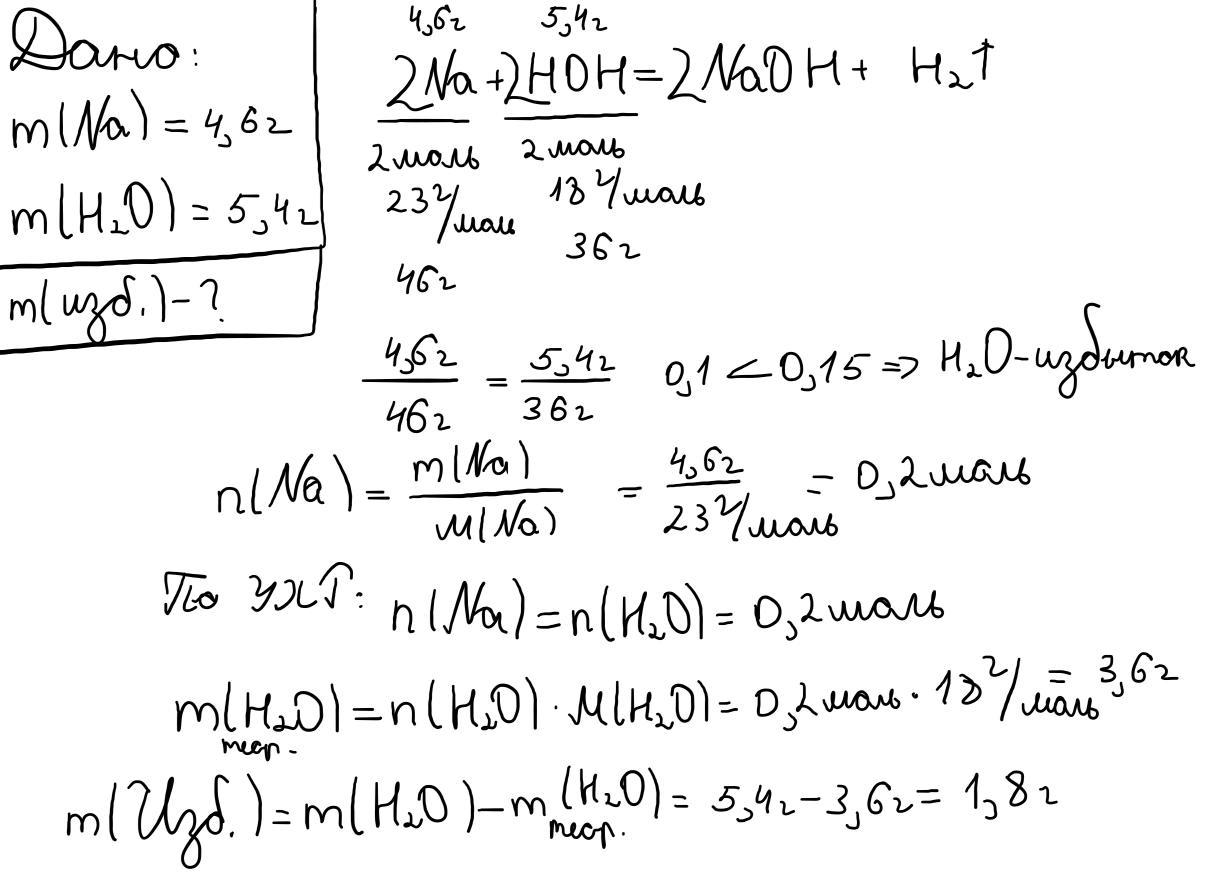
Ответ дал:
1
Ответ: избыточное вещество вода с массой 1,8 г
Объяснение:
Дано:
m(Na) = 4,6 г
m(H2O) = 5,4 г
Найти: m(изб.) - ?
Составим УХР:
2Na + 2H2O = 2NaOH + H2
Вычислим количество вещества реагентов:
n(Na) = m(Na)/ M(Na) = 4,6/23 = 0,2 моль
n(H2O) = m(H2O)/ M(H2O) = 5,4/ 18 = 0,3 моль
Из УХР видим, что n(Na) : n(H2O) = 2 : 2 = 1 : 1 , а из условия
n(Na) : n(H2O) = 0,2 : 0,3 то есть вода в избытке расчет ведем по натрию n(H2O) = n(Na) = 0,2 моль
mтеор.(H2O) = n(H2O) * М(Н2О) = 0,2 * 18 = 3,6 г
m(изб.) = m(H2O) - mтеор.(H2O) = 5,4 - 3,6 = 1,8 г
Вас заинтересует
2 года назад
2 года назад
2 года назад
2 года назад
3 года назад
3 года назад
9 лет назад